Диверсионный колит эндоскопия признаки
Полный текст статьи:
Диверсионный[Оэ1] колит
М.С. Аникина, врач-эндоскопист ГБУЗ НСО «Государственная Новосибирская областная клиническая больница», Новосибирск, 2018 год
Аннотация. В отключенных сегментах толстой кишки после хирургических вмешательств с наложением различного типа стом развивается неспецифическое воспаление, которое носит название диверсионного колита, или колита отключенной кишки. Проведение колоноскопии этой группе пациентов — неотъемлемая часть рутинной практики врача-эндоскописта. В обзоре рассмотрены вопросы эпидемиологии, патогенеза, эндоскопической семиотики диверсионного колита, а также подготовка к колоноскопии пациентов, перенесших операции на толстой и прямой кишке.
Введение. На сегодняшний день в хирургической практике широко используются многоэтапные вмешательства, которые улучшают непосредственные результаты лечения и приводят к снижению числа осложнений и послеоперационной летальности. Показаниями к таким вмешательствам могут служить злокачественные новообразования, дивертикулярная болезнь, аномалии развития толстой кишки и другое. Однако в результате наложения колостомы или илеостомы в отключенных сегментах толстой кишки развивается неспецифическое воспаление, называемое диверсионным колитом, или колитом отключенной кишки [1]. Впервые это патологическое состояние было описано V. Morson в 1974 году, но термин «диверсионный колит» был введен D. Glotzer в 1981-м [1, 3, 8, 9].
Эпидемиология. Распространенность диверсионного колита у стомированных пациентов чрезвычайно высока и составляет 74–91% [1, 3, 9]. Считается, что у пациентов с предшествующим хроническим воспалительным заболеванием кишечника (ХВЗК) частота развития диверсионного колита выше, но, согласно результатам исследования Son и соавторов о диверсионном колите у пациентов, оперированных по поводу рака прямой кишки, частота развития составила 100% [7, 8]. Связи между диверсионным колитом, возрастом, полом, типом стомы или способом выполненного оперативного вмешательства нет [3, 9].
Патогенез. Основные механизмы, лежащие в основе диверсионного колита, по-прежнему до конца не ясны. Главное звено в патогенезе этого заболевания — бактериальный дисбаланс, развивающийся вследствие нарушения нормального пассажа кала, который приводит к нарушению защитной функции слизистой оболочки и снижению количества короткоцепочечных жирных кислот (КЦЖК). КЦЖК участвуют в метаболизме колоноцитов, покрывая около 70% их энергетических потребностей, и недостаток этих кислот приводит к нарушению энергетического обмена в эпителии толстой кишки [1]. С другой стороны, КЦЖК расслабляют гладкие мышцы сосудов — и их дефицит может вызывать повышение тонуса сосудов, что приводит к относительной ишемии слизистой и стенки толстой кишки (ишемическая теория) [9]. Основные теории патогенеза диверсионного колита представлены на рис. 1.
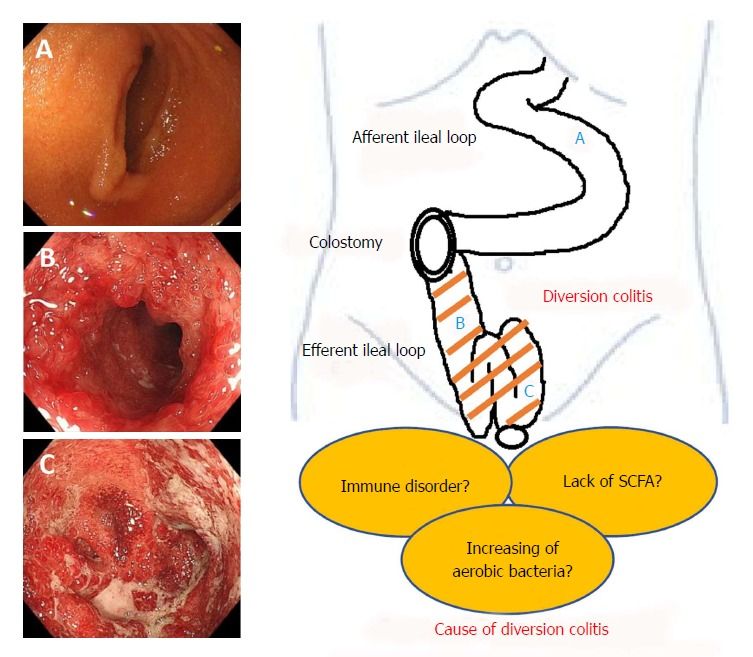
Рис. 1. Основные теории патогенеза диверсионного колита [9].
Клиническая картина. Клинические проявления возникают примерно у 30% больных без ХВЗК, но у пациентов с болезнью Крона встречаются в 33% случаев, а при язвенном колите — 87%.[Оэ2] Симптомы диверсионного колита возникают в течение 1–36 месяцев после наложения колостомы [3, 9]. Пациенты с диверсионным колитом жалуются на выделение слизи и/или крови, тенезмы, боли в животе, чувство тяжести или боль в прямой кишке [1, 7]. Патологические выделения из прямой кишки — наиболее распространенный симптом (40%), на втором месте по встречаемости — боли в животе и тенезмы (15%) [9]. Наиболее информативный в этом случае диагностический метод — ректороманоскопия и колоноскопия с гистологическим исследованием биоптата слизистой и удаленных операционных препаратов из отключенных отделов ободочной и прямой кишки [1].
Эндоскопическая картина. Макроскопические изменения в отключенной толстой кишке могут носить как непрерывный, так и сегментарный характер [9]. Диверсионный колит представлен отеком, зернистостью, петехиальными кровоизлияниями, контактной кровоточивостью слизистой, смазанностью сосудистого рисунка и напоминает эндоскопическую картину язвенного колита с умеренной степенью активности [1].
Пристеночно отмечаются налеты слизи. Son с соавторами в своей работе оценивали по эндоскопической картине в отдельности выраженность отека (0–3 балла), внутрислизистых кровоизлияний (0–3 балла) и контактную кровоточивость (0–1 балл). Впоследствии баллы суммировались (0–7 баллов). По общему баллу диверсионный колит был разделен на слабый (0–2 балла), умеренный (3–5 баллов) и тяжелый (6–7 баллов) (рис. 2) [8].
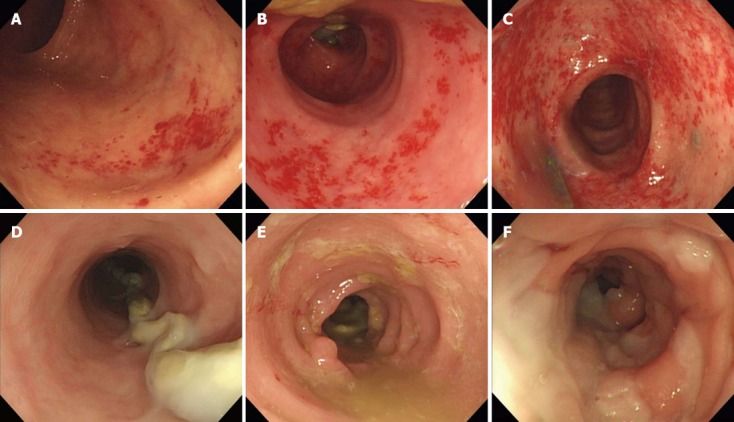
Рисунок 2. Эндоскопические проявления диверсионного колита [8].
Пример основных эндоскопических результатов при диверсионном колите в зависимости от относительной тяжести.
A, B, C. Петехиальные кровоизлияния (A — 1 балл; B — 2 балла; C — 3 балла).
D, E, F. Отек (D — 1 балл; E — 2 балла; F — 3 балла).
Подготовка к колоноскопии пациентов, перенесших операцию на толстой кишке. Мною найдено небольшое количество ресурсов, посвященных проблеме подготовки данной группы пациентов. В отечественной литературе эта проблема освещена крайне скудно.
Пациентам с разгрузочными илеостомами прием пероральных препаратов для очистки кишечника не показан. Таким больным проводят промывание толстой кишки через илеостому, которое может быть дополнено очистительными клизмами, это обычно требует госпитализации в хирургическое отделение [12]. На сайте gnck.ru уточняется, что специальная подготовка пациентам с разгрузочной илеостомой не показана [13]. Однако в нашей практике мы довольно часто наблюдаем неадекватную подготовку толстой кишки к исследованию даже после проведения очистительных клизм. Для пациентов с петлевой колостомой рекомендуется проведение стандартной подготовки пероральными препаратами для очистки кишечника в комбинации с промыванием отключенных отделов через колостому. Пациенты с концевыми колостомами (после операций типа Гартмана) должны проходить стандартную подготовку пероральными препаратами для очистки кишечника в комбинации с очистительными клизмами. Пациентам после субтотальной резекции рекомендована одноэтапная быстрая подготовка с последующей очистительной клизмой — как для сигмоскопии. Нестомированным пациентам после различных вариантов резекции толстой и прямой кишки и брюшно-анальной резекции показана стандартная пероральная подготовка [12].
На сегодняшний день стандартной считается двухэтапная подготовка или одноэтапная в день исследования полным объемом полиэтиленгликоля. Исследование Liu и соавторов показало, что уменьшение стандартного объема ПЭГ с 4 л до 2 л в сплит-режиме у пациентов с оперированной толстой кишкой приводит к снижению качества подготовки (89,4% против 66,7%, P < 0,001) [6].
Действенная альтернатива полнообъемным препаратам ПЭГ — применение малообъемного препарата ПЭГ с аскорбатным комплексом («МОВИПРЕП®»). Применение препарата «МОВИПРЕП®» предпочтительнее для амбулаторных пациентов, сопряжено с меньшим количеством таких нежелательных явлений, как тошнота и рвота, а также с большей приверженностью пациентов [2, 4, 5, 10, 11]. В проведенном многоцентровом рандомизированном клиническим исследовании в России по оценке подготовки пациентов по утренней и двухэтапной схеме применения препарата МОВИПРЕП®, показано, что обоих схемах наблюдается почти в 100% случаях эффективная подготовка кишечника, включая правые отделы [14].
Гистологическая картина. Гистологические изменения в отключенной кишке присутствуют у всех стомированных пациентов [1, 8, 9]. В биоптатах слизистой при диверсионном колите выявляются признаки острого или хронического воспаления, эозинофильная инфильтрация, нарушение архитектоники крипт, фолликулярная лимфоидная гиперплазия и крипта-абсцессы [1, 8, 9]. Son и соавторы [8] также использовали шкалу оценки тяжести диверсионного колита, оценивая эти признаки по отдельности: острое воспаление (0–1 балл); хроническое воспаление (0–2 балла); эозинофильная инфильтрация (0–2 балла); нарушение архитектоники крипт (0–1 балл); фолликулярная гиперплазия (0–1 балл); крипта-абсцессы (0–1 балл) — с возможной суммой общего балла от 0 до 8. По общему баллу диверсионный колит был разделен на слабый (1–3 балла), умеренный (4–6 баллов) и тяжелый (7–8 баллов) (см. рис. 3).
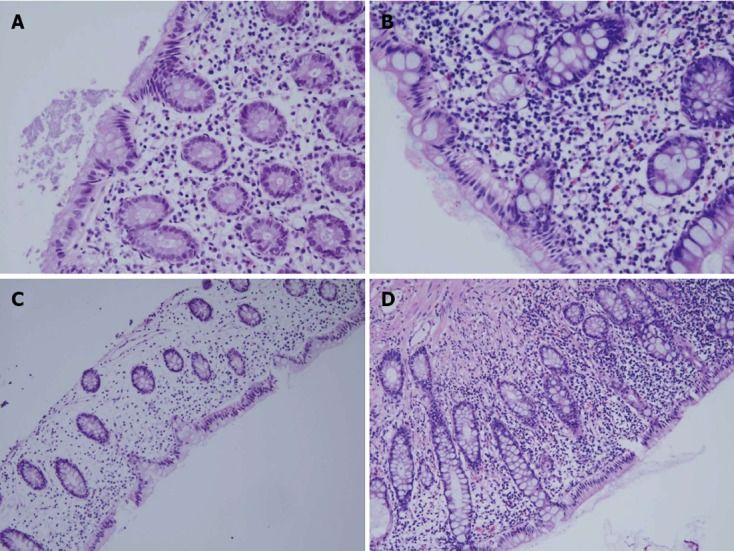
Рисунок 3. Гистологическая картина диверсионного колита [8].
Пример основных гистологических результатов при диверсионном колите в зависимости от относительной тяжести.
А, B. Эозинофильная инфильтрация (A — 1 балл; B — 2 балла; окраска гематоксилином и эозином, увеличение 400x).
C, D. Хроническое воспаление с мононуклеарными макрофагами, лимфоцитами и плазматическими клетками (C — 1 балл; D — 2 балла; окраска гематоксилином и эозином, увеличение 200x).
Лечение. Цель лечения — уменьшение или устранение симптомов [3, 9]. Ликвидация коло- либо илеостомы приводит к излечению, однако Son с соавторами указывают, что у пациентов с тяжелым диверсионным колитом после ликвидации стомы может возникнуть диарея [8]. Фармакологические методы лечения необходимы для симптомных пациентов с постоянными стомами и пациентов, у которых ликвидация стомы не может быть проведена по причинам технических трудностей, плохой функции анального сфинктера или стойкого перианального сепсиса. На сегодняшний день не существует единых подходов к терапии диверсионного колита у таких пациентов. Используются препараты КЦЖК, 5-аминосалициловой кислоты, клизмы с кортикостероидами или волокнами [1, 3, 9]. Существуют единичные сообщения о применении фекотрансплантации [9] и спрея декстрозы [7, 9].
Выводы
Диверсионный колит – неспецифическое воспаление, возникающее в отключенной кишке после наложения стомы. Данное состояние развивается у всех стомированных пациентов, но при этом симптомы (выделение слизи и/или крови, тенезмы, боли в животе, чувство тяжести или боль в прямой кишке) возникают только у 30% человек. Диагностика диверсионного колита основана на данных колоноскопии с гистологическим исследованием биоптата. Эндоскопические признаки диверсионного колита: отек, зернистость, петехиальные кровоизлияния, контактная кровоточивость слизистой, смазанность сосудистого рисунка. Гистологическая картина представлена признаками острого или хронического воспаления, эозинофильной инфильтрацией, нарушением архитектоники крипт, фолликулярной лимфоидной гиперплазией и крипта-абсцессами. Основной метод лечения диверсионного колита – ликвидация стомы. Единых подходов к медикаментозному лечению на сегодняшний день нет.
Список литературы
1. Воробьев Г.И., Жученко А.П., Филон А.Ф., Китчиева Г.М. Колит отключенной толстой кишки (обзор литературы) // РЖГГК. — 2008. — Т. 18. — №5. — С. 65–70.
2. Hassan C., Bretthauer M., Kaminski M.F., Polkowski M., Rembacken B., Saunders B., Benamouzig R., Holme O., Green S., Kuiper T., Marmo R., Omar M., Petruzziello L., Spada C., Zullo A., Dumonceau J.M.; European Society of Gastrointestinal Endoscopy. Bowel preparation for colonoscopy: European Society of Gastrointestinal Endoscopy (ESGE) guideline. Endoscopy. 2013. 45 (2): 142–150. Epub 2013 Jan 18. PMID: 23335011. DOI: 10.1055/s-0032-1326186.
3. Kabir S.I., Kabir S.A., Richards R., Ahmed J., MacFie J. Pathophysiology, clinical presentation and management of diversion colitis: a review of current literature. Int J Surg. 2014. Oct; 12 (10): 1088–1092. Epub 2014 Aug 20. PMID: 25150021. DOI: 10.1016/j.ijsu.2014.08.350.
4. Kim E.S., Kim K.O., Jang B.I., Kim E.Y., Lee Y.J., Lee H.S., Jeon S.W., Kim H.J., Kim S.K.; Crohn’s and Colitis Association in Daegu-Gyeongbuk (CCAiD). Comparison of 4-L Polyethylene Glycol and 2-L Polyethylene Glycol Plus Ascorbic Acid in Patients with Inactive Ulcerative Colitis. Dig Dis Sci. 2017. Sep; 62 (9): 2489–2497. Epub 2017 Jun 21. PMID: 28639128. DOI: 10.1007 / s10620-017-4634-7.
5. Kojecky V., Dastych M., Zadorova Z., Varga M., Hajer J., Kment M., Kroupa R., Kunovska M., Matous J., Misurec M., Hep A., Kianicka B., Latta J. [Effective bowel preparation before coloscopy — low-volume PEG in the divided dose regimen]. Vnitr Lek. 2016. Apr; 62 (4): 249–254. PMID: 27250601.
6. Liu Z., Li Y.Y., Luo X.T., Guo C.G., Zhang M.M., Li Z., Li L.X., Zhang Y., Li Y.Q. Split-dose 4-L polyethylene glycol regimen for patients with previous colorectal surgery in bowel preparation before colonoscopy: A randomized, controlled, single-blind study. J Dig Dis. 2018. Jun; 19 (6): 359–368. DOI: 10.1111/1751-2980.12608.
7. Nyabanga C.T., Shen B. Endoscopic Treatment of Bleeding Diversion Pouchitis with High-Concentration Dextrose Spray. ACG Case Rep J. 2017. Mar 29; 4: e51. eCollection 2017. PMID: 28377939. PMCID: PMC5371723. DOI: 10.14309/crj.2017.51.
8. Son D.N., Choi D.J., Woo S.U., Kim J., Keom B.R., Kim C.H., Baek S.J., Kim S.H. Relationship between diversion colitis and quality of life in rectal cancer. World J Gastroenterol. 2013. Jan 28; 19 (4): 542–549. PMID: 23382634. PMCID: PMC3558579. DOI: 10.3748/wjg.v19.i4.542.
9. Tominaga K., Kamimura K., Takahashi K., Yokoyama J., Yamagiwa S., Terai S. Diversion colitis and pouchitis: A mini-review. World J Gastroenterol. 2018. Apr 28; 24 (16): 1734–1747. PMID: 29713128. PMCID: PMC5922993. DOI: 10.3748/wjg.v24.i16.1734.
10. Xie Q., Chen L., Zhao F., Zhou X., Huang P., et al. A Meta-Analysis of Randomized Controlled Trials of Low-Volume Polyethylene Glycol plus Ascorbic Acid versus Standard-Volume Polyethylene Glycol Solution as Bowel Preparations for Colonoscopy. PLoS One. 2014. Jun 5; 9 (6): e99092. DOI:10.1371/journal.pone.0099092.
11. Zorzi M., Valiante F., Germana B., Baldassarre G., Coria B., Rinaldi M., Heras Salvat H., Carta A., Bortoluzzi F., Cervellin E., Polo M.L., Bulighin G., Azzurro M., Di Piramo D., Turrin A., Monica F.; TriVeP Working Group. Comparison between different colon cleansing products for screening colonoscopy. A noninferiority trial in population-based screening programs in Italy. Endoscopy. 2016. Mar; 48 (3): 223–231. Epub 2016 Jan 13. DOI: 10.1055/s-0035-1569574.
12. Bowel Prep Protocol | Colonoscopy | Gastroenterology // 16.11.2018.
13. gnck.ru›rehabilitation.shtml // 16.11.2018.
14. Веселов В.В., Сидоров А.В., Василюк В.Б., Гордиенко А.В., Меньшикова И.Л., Симаненков В.И., Щербаков П.Л. Малообъемный раствор препарата ПЭГ с аскорбиновой кислотой для подготовки к колоноскопии по одноэтапной утренней или стандартной двухэтапной (сплит) схемам: многоцентровое простое слепое рандомизированное контролируемое исследование в параллельных группах. Колопроктология. №2 (60). 2017. — C. 5-18
[Оэ2] ХВЗК представлены болезнью Крона и язвенным колитом. У пациентов с данными заболеваниями клинические проявления бывают чаще, чем у пациентов с другой патологией.
Источник