Этиология патогенез язвенного колита
 Воспалительное заболевание кишечника
Воспалительное заболевание кишечникаВоспалительное заболевание кишечника (ВЗК) – это идиопатическая, дизрегуляционная, рецидивирующая и ослабляющая иммунная реакция на кишечную микрофлору хозяина, вызванная сочетанием множества факторов, включая генетику, экологию и физиологию.
Недавние исследования пролили свет на значительную роль врожденной иммунной системы в возникновении дисбаланса между полезной и патогенной кишечной микрофлорой. Другими словами, иммунитет должен защищать хозяина от инородных тел, патогенов и инфекций, но при ВЗК он ошибочно принимает полезные бактерии, продукты питания и другие безвредные элементы за враждебные и атакует кишечник. Этот процесс приводит к высвобождению лейкоцитов в этих местах и активации воспалительного процесса.
Язвенный колит и болезнь Крона
Существуют две формы воспалительного заболевания кишечника – язвенный колит и болезнь Крона. Несмотря на то, что обе эти патологии имеют схожую симптоматику, основное различие между ними заключается в местоположении и характере вызванного воспаления.
Язвенный колит (НЯК) – это хроническое заболевание толстой кишки, характеризующееся иммунным воспалением ее слизистой оболочки. В отличие от болезни Крона, воспалительный процесс при язвенном колите ограничен только толстым кишечником. Как правило, НЯК начинается с легких симптомов (например, капель крови в стуле), которые постепенно прогрессируют до более тяжелых, с периодами ремиссии между ними. Наиболее распространенным проявлением язвенного колита являются частая диарея с примесью крови, боли в животе и повышение температуры тела. Потеря аппетита, усталость и потеря веса являются следствием вышеобозначенных симптомов. Однако, в отличие от болезни Крона, периоды ремиссии у пациентов с НЯК более длительные. Пациенты с язвенным колитом подвергаются повышенному риску рака толстой кишки.
 Слои стенки кишечника
Слои стенки кишечника
Болезнь Крона (БК) – это хроническое воспалительное заболевание желудочно-кишечного тракта, которое может поражать все его отделы, начиная от полости рта и заканчивая прямой кишкой. Чаще всего болезнь Крона затрагивает тонкий кишечник, иногда распространяясь на верхние слои толстой кишки. Воспаление при БК чаще всего бывает трансмуральным, т.е. затрагивающим все слои кишечной стенки (слизистую оболочку, подслизистую основу, мышечный слой и серозную оболочку), и прерывистым (чередуясь со здоровыми участками тканей). К симптомам болезни Крона относятся постоянная диарея (иногда с примесями крови), нерегулярные и частые позывы к дефекации, потеря веса, общее недомогание и усталость. Наиболее распространенным осложнением, характерным для БК, является кишечная непроходимость, возникающая вследствие избыточного воспаления и отека стенок кишечника и приводящая к спазмам в животе, вздутию и рвоте. Болезнь Крона также часто сопровождается свищами, что повышает риск инфицирования больного.
Как БК, так и НЯК могут перейти в такую стадию, при которой консервативное лечение уже станет бесполезно, и придется прибегнуть к хирургическому вмешательству.
Большинство симптомов язвенного колита и болезни Крона в обоих случаях очень похожи. К характерным признакам ВЗК, именно вследствие пагубного воздействия заболевания на организм, относятся так называемые внекишечные проявления язвенного колита и болезни Крона. К ним относятся оральные афты (язвы во рту), узловатая эритрема, артрит, эписклерит и другие. Именно из-за этих неспецифических симптомов дифференцировать НЯК и БК в ряде случаев становится очень сложно. Медицинский термин для обозначения этого состояния – недифференцируемый колит (НК)
ВЗК не следует путать с синдромом раздраженного кишечника (СРК), вся суть которого – в “неконтроллируемых и беспорядочных” сокращениях кишечника. Основное и самое главное отличие ВЗК от СРК – отсутствием при второй патологии органических поражений стенок органов желудочно-кишечного тракта.
Этиология НЯК и БК
Пациенты с воспалительным заболеванием кишечника обычно имеют генетическую предрасположенность, но на сегодняшний день нет единственно верного фактора, который можно было бы назвать ответственным за возникновение этой патологии. Принято считать, что именно сочетание генетических, патогенных (иммунологических), физиологических (в том числе питания и образа жизни) и экологических моментов может послужить причиной развития язвенного колита или болезни Крона.
Среди ряда этиологических теорий, постулируемых как возможные причины ВЗК, наиболее заметными из них являются:
- Дисбаланс кишечной микрофлоры, приводящий к стойкой инфекции (вирус в клетке размножается, но вирусные частицы постепенно покидают клетку-хозяина, не разрушая, а изменяя ее функционирование)
- Неправильная иммунорегуляция.
Однако, в последнее время участились случаи публикации доказательств в пользу, все-таки, генетической природы ВЗК. Подробнее о них вы можете узнать из новостей на этом сайте.
Болезнь Крона
Одним из основных генов, подлежащих изучению в связи с развитием БК, является CARD15 (член семейства домена каспазы, ранее известный как NOD2). Этот ген отвечает за распознавание клеточной стенки бактерий, которая, в свою очередь, кодирует NF-κB (ядерный фактор), медиатор провоспалительных цитокинов и защитных молекул (например, антимикробных пептидов), который обрабатывает чужеродный антиген и обеспечивает гомеостаз. На сегодняшний день найдены три одиночных нуклеотидных полиморфизма (SNP-мутации), которые приводят к увеличению числа комменсальных бактерий в кишечнике, ошибочной регуляции врожденной иммунной системы (активация NF-κB) и неэффективному избавлению от патогенных бактерий.
Другим геном, изученным на предмет его роли в этиологии болезни Крона, является IL-23R, который отвечает за синтез белка рецептора интерлейкина 23 (IL-23). Этот регуляторный белок играет важную роль в организме человека, поскольку он присутствует на поверхности большинства иммунных клеток (Т-клетки, естественные клетки-убийцы, моноциты и дендритные клетки) и опосредует провоспалительные пути против патогенов. Он делает это путем связывания с IL-23, мощным провоспалительным цитокином, который приводит к иммунной реакции против вторгающихся патогенов. IL-23R также отвечает за регулирование синтеза IL-17 путем активации лимфоцитов Th17 из клеток памяти и способствует их выживанию. Изучение животных моделей с подавленным IL-23R показало увеличение и неконтролируемый синтез провоспалительных цитокинов IL-23 и IL-17, что поспособствовало развитию у подопытных мышей симптоматики, схожей с воспалительными заболеваниями кишечника. Из этого можно сделать вывод, что мутация в IL-23R является одной из причин развития болезни Крона.
Гены, участвующие в аутофагии, также изучались на предмет их взаимосвязи с БК. Аутофагия – это процесс, обычно участвующий в уничтожении нежелательных или потенциально опасных внутренних клеточных компонентов. Если ген, ответственный за аутофагию, мутирован, это может вызвать дисбаланс в отношении безвредной симбиотической и вредной инвазивной патогенной флоры и вызвать проблемы в желудочно-кишечном тракте, предрасполагая тем самым к болезни Крона. Белок ATG16L1 отвечает за синтез одного из таких генов, и мутация этого белка связана с развитием илеита (формы болезни Крона, при котором поражается подвздошная кишка)
Помимо CARD15, IL-23R и ATG16L1, развитию БК способствует мутация в генах TNFSF15, CTLA4 и IBD5.
Язвенный колит
На данный момент роль генетики в развитии язвенного колита доказана в куда меньшей степени, чем в случае с болезнью Крона. Было обнаружено, что гены, подобные DLG5, которые отвечают за поддержание целостности стенки кишечника, способствуют повышению предрасположенности к НЯК и БК. Помимо DLG5, ген MDR1, кодирующий множественную лекарственную устойчивость и перенос амфипатических веществ через мембраны, также показал повышенную восприимчивость к развитию язвенного колита. Ген ECM1, кодирующий белок 1 внеклеточного матрикса, ответственный за поддержание целостности кожи и ее и гомеостаза, также изучается на предмет отношения к НЯК.
Среди населения Японии было проведено несколько исследований, в которых изучались генетические мутации некоторых человеческих лейкоцитарных антигенов (Human Leukocyte Antigens, HLA). Выяснилось, что один из антигенов, снижая риск развития одного типа ВЗК, одновременно с этим повышал предрасположенность к другому. Однако, в случае европейских популяций, такие случаи были весьма редки.
В исследованиях, проводимых в Северной Америке и Европе, было показано, что генетические предрасположенности затрагивают больше детей, нежели взрослых. Это может быть связано с тем, что иммунная система проходит этапы становления именно в юном возрасте, и в этот период она более подвержена риску возникновения тех или иных сбоев.
Факторы риска развития воспалительных заболеваний кишечника
- Семейная предрасположенность. У людей, у которых в роду кто-то болел НЯК или БК, особенно родственники “первой линии” (отец и мать), повышается риск развития воспалительного заболевания кишечника. У ребенка есть шанс в примерно 5% “заполучить” ВЗК от родителей. Если одному из близнецов диагностировали язвенный колит или болезнь Крона, с вероятностью 70% эта же участь ждет и другого ребенка. В случае с двойняшками, статистика говорит о 5-10% “распространения” на них заболевания от своего брата/сестры.
- Курение. Курение – один из основных факторов риска, способствующих развитию ВЗК. Риски развития БК повышаются у “текущих” курильщиков, тогда как шанс заполучить НЯК увеличивается при отказе человека от этой вредной привычки.
- Этничность. Воспалительные заболевания кишечника распространены в основном в североамериканских и европейских, и наименее в азиатских и африканских странах. Очень склонны к развитию ВЗК кавказцы и евреи. Как было установлено, промышленно развитые страны имеют более высокую распространенность ВЗК. Урбанизация и вестернизация подвергает людей опасным последствиям (промышленный дым, загрязнение, аллергены и т.д.), которые выступают в качестве предрасполагающих факторов для развития НЯК или БК.
- Лекарственные препараты. Использование определенных лекарств может увеличить риск развития ВЗК. К ним относятся Изотретиноин, Аспирин, Ибупрофен, Напроксен и прочие. Нестероидные противовоспалительные средства (НПВС) могут способствовать образованию язв в желудочно-кишечном тракте, что как способствует ВЗК, так и усложняет его лечение.
- Возраст и пол. ВЗК в основном поражает людей в возрасте от 21 до 30 лет (как можно судить из статистики). Согласно Центру по контролю и профилактике заболеваний США, распространенность НЯК выше среди мужчин, а БК – среди женщин.
Эпидемиология язвенного колита и болезни Крона
Значительный рост числа случаев ВЗК в Северной Америке и Европе произошел со второй половины двадцатого века. Места с более холодным климатом и урбанизацией, как правило, имеют более высокую заболеваемость НЯК и БК.
В связи с тем, что точная распространенность ВЗК не может быть отражена из-за отсутствия “золотого стандарта” диагностики и ошибочной классификации состояния, приблизительная оценка, основанная на многочисленных исследованиях, показывает, что от язвенного колита и болезни Крона страдают от 70 до 150 человек на 100000 населения. Распространенность для БК колеблется от 319 / 100000 в Северной Америке до 322 / 100000 в Европе, а для НЯК – от 249 / 100000 в Северной Америке и до 505 / 100000 в Европе. На международном уровне распространенность язвенного колита составляет от 0,5 до 24,5 / 100000, а для БК – от 0,1 до 16 / 100000, причем распространенность ВЗК в целом составляет приблизительно 396 / 100000. К этим данным стоит отнестись скептически, т.к. в ряде случаев людям просто-напросто ставят неправильный диагноз.
Частота случаев болезни Крона является самой высокой в Северной Америке, за ней следуют Европа, затем – Азия и Ближний Восток. Частота заболеваемости язвенным колитом самая высокая в Европе, далее, в порядке убывания – в Северной Америке, на Ближнем Востоке и в Азии.
Патофизиология НЯК и БК
Воспалительное заболевание кишечника традиционно определяется как “абберантный ответ иммунной системы на внутрипросветные антигены бактериального происхождения у генетически предрасположенных людей”. Исследования говорят о том, что больше, чем патогенетический аспект, патофизиология ВЗК в большей степени зависит от дефектной врожденной иммунной системы, которая неспособна регулировать иммунные реакции, что приводит к избыточному воспалению и составляет саму суть язвенного колита и болезни Крона.
Врожденная иммунная система образует первую линию защиты от патогенов, борясь с ними в зависимости от их химической природы. Клетки врожденной иммунной системы включают в себя медиаторы, такие как цитокины, молекулы адгезии, хемокины и лимфоциты, которые ответственны за “настройку” воспалительных клеток на чужеродного агента, регулируют реакции эффекторных клеток и представляют антигены адаптивной иммунной системе, для их дальнейшей обработки и уничтожения. Предполагается, что отказ регуляторных цитокинов, высвобождаемых врожденной иммунной системой, таких как IL-10, IFNγ и TGFβ поспособствует развитию сильного воспаления. Исследования показали, что в этом случае Т-лимфоциты (в основном Т-хелперы) не подвергаются апоптозу, поскольку антитела против IL-12 и ФНО не синтезируются (IL-12 и ФНО являются двумя наиболее сильными провоспалительными цитокинами), что способствует воспалению. Исследование, связанное с мутациями гена NOD2 (CARD15), который является еще одним триггером для регулирования врожденной иммунной системы, выступает еще одним доказательством того, что у людей с воспалительным заболеванием кишечника в какой-то момент их жизни происходит сбой в работе врожденного иммунитета.
Еще одной важной частью врожденной иммунной системы является эпителий кишечника: слизистые железы обеспечивают иммунитет против патогенов, поддерживают гомеостаз слизистой оболочки, а также образуют защитное покрытие кишечника. Генетические предрасположенности могут повлиять на целостность этого барьера, что делает кишечник легкодоступным для заражения комменсальными микроорганизмами из других источников (например, из кала) и приводит к ошибочной активации иммунной системы.
Что касается эффекторных иммунных реакций, то хелперные Т-лимфоциты не подвергаются апоптозу после их синтеза цитокинами. Цитокины Th1 (IL-12, IFNγ, ФНО) вносят вклад в развитие болезни Крона, тогда как появление у человека язвенного колита объясняется преимущественно Th2 цитокинами (IL-4 и IL-5). Тем не менее, эта теория также была поставлена под сомнение недавними исследованиями, которые показали, что терапия ингибиторами ФНО привела к индуцировании ремиссии НЯК. Кроме того, в некоторых случаях язвенного колита также наблюдалось увеличение популяции IL-13. В связи с этим, подавление IL-13 в будущем может лечь в основу создания новых препаратов для лечения НЯК. Было установлено, что антитела против ФНО и IL-10 вызывают ремиссию БК в куда меньших случаях, чем при НЯК, что указывает на вовлечение в ВЗК смешанных профилей цитокинов.
Язвенный колит начинается в прямой кишке и со временем может распространиться на весь толстый кишечник. Прямая кишка всегда является частью НЯК. В 25% случаев заболевание так и остается локализованным в самой прямой кишке. Примерно 10-12% случаев язвенный колит затрагивает все части толстого кишечника. Периоды обострения сопровождаются сравнительно более длительными периодами ремиссии, чем при болезни Крона.
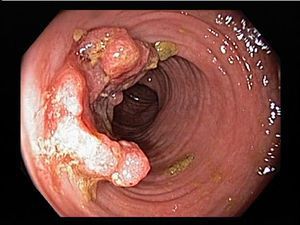
Ранняя стадия заболевания характеризуется возникновением псевдополипов. В более тяжелых состояниях на слизистой оболочке кишечника появляются язвы с гнойными экссудатами, часто содержащие в себе бактерии, которые усугубляют течение заболевания. В крайних случаях толстый кишечник утрачивает свою мускулатуру и неограниченно расширяется, приводя к так называемому токсическому колиту, что может привести к перфорации. Люди с НЯК подвергаются повышенному риску развития колоректального рака.
Болезнь Крона, в отличие от НЯК, может начаться в любой части желудочно-кишечного тракта и распространиться в любое его место, начиная от рта и заканчивая прямой кишкой. БК в основном поражает подвздошную кишку и толстый кишечник и имеет три формы – воспаление, стриктуры и свищи. В зависимости от места воспаления различают следующие типы болезни Крона:
- Илеоколит (с участием подвздошной кишки и толстой кишки, 35-45% случаев).
- Илеит (только подвздошная кишка, 35% случаев).
- Гранулематозный колит (только толстый кишечник, 32% случаев).
- Еюнит (тощая кишка, 28% случаев).
- Дуоденит (двенадцатиперстная кишка, 5% случаев).
 Иллюстрация “булыжной мостовой” при БК
Иллюстрация “булыжной мостовой” при БК
Состояние начинается с аномального воспаления и распространяется трансмурально, воздействуя на лимфатические узлы и сосуды и вызывая утолщение стенки кишечника. Гипертрофия мускулатуры слизистой оболочки и формирование стриктур (сужение просвета кишечника) является обычным явлением при БК. Поражения слизистой оболочки происходит путем чередования сильно и слабо воспаленных участков, формируя тем самым вид “булыжной мостовой”. Фистулы (образование аномальных связей между кишечником и другими соседними органами) образуют еще одну общую особенность болезни Крона. Хирургическое вмешательство (в основном из-за осложнений, вызванных заболеваниями) чаще встречается при БК (около 75% случаев, требующих хирургического вмешательства), чем при НЯК (25%). Как и в случае с язвенным колитом, поражение толстого кишечника при болезни Крона также связывают с повышенным риск развития колоректального рака. Также, в ряде случаев при БК наблюдается формирование абсцессов и некротизирующих опухолей.
Источник
Дата публикации 11 мая 2018 г.Обновлено 22 июля 2019 г.
Неспецифический язвенный колит (или просто язвенный колит) — хроническое воспаление толстой кишки аутоиммунного характера. Данное заболевание относится к группе воспалительных заболеваний толстого кишечника.
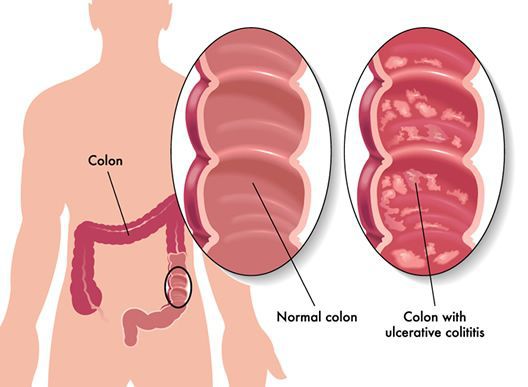
Эпидемиология
Заболевание преобладает в развитых странах Европы и Северной Америки. Язвенный колит встречается в 20-260 случаев на 100 000 человек. С каждым годом число заболевших увеличивается.[2]
Чаще всего болеют лица в возрасте от 21 до 42 лет, а также пациенты после 54 лет. Самые опасные периоды в развитии язвенного колита — это первый год болезни (из-за быстрого развития воспаления при фульминантном течении появляются осложнения, опасные для жизни) и десятый год (за этот период развиваются злокачественные новообразования).
Факторы риска до сих пор до конца не изучены. Существует следующая закономерность:
- Взаимосвязь курения и язвенного колита. По статистическим данным курящие люди реже болеют язвенным колитом.
- Аппендэктомия (удаление аппендицита) в анамнезе снижает заболеваемость язвенным колитом.
- Снижение количества пищевых волокон способствует появлению болезни.
- Лица, чаще болеющие детскими инфекциями, имеют склонность к появлению данного заболевания.
Этиология
Происхождение язвенного колита на сегодняшний день неизвестно. Существуют следующие теории развития заболевания:
- Язвенный колит возникает под действием определённых экзогенных (внешних) факторов, которые не известны. Предположительной причиной является инфекция.
- Заболевание имеет аутоиммунный характер. Существует наследственная предрасположенность к развитию болезни. Под воздействием определённых факторов запускаются иммунные реакции, вырабатываются антитела, направленные на клетки толстого кишечника.
- Язвенный колит развивается вследствие реакции организма на определённые продукты питания, при этом воспаляется кишечная стенка.
Основными симптомами заболевания являются:
- кишечные кровотечения;
- диарея;
- запор;
- боль в животе;
- тенезмы (ощущение постоянных режущих, тянущих, жгучих болей в толстой кишке — позывов к дефекации, однако при этом выделение кала не происходит);
- лихорадка;
- снижение массы тела;
- тошнота, рвота;
- слабость;
- внекишечные симптомы (артрит, узловатая эритема, увеит и другие).
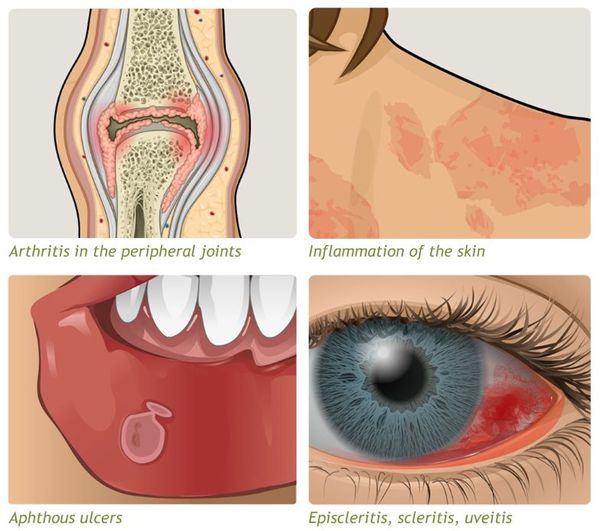
Характер преобладающей симптоматики зависит от тяжести заболевания и вовлечённого в воспалительный процесс отдела толстого кишечника. Например, при тотальном поражении наблюдается частый жидкий стул с большим количеством крови в кале, боли в животе спастического характера. При тяжёлом течении присоединяются симптомы общей интоксикации (лихорадка, тошнота, рвота, слабость).
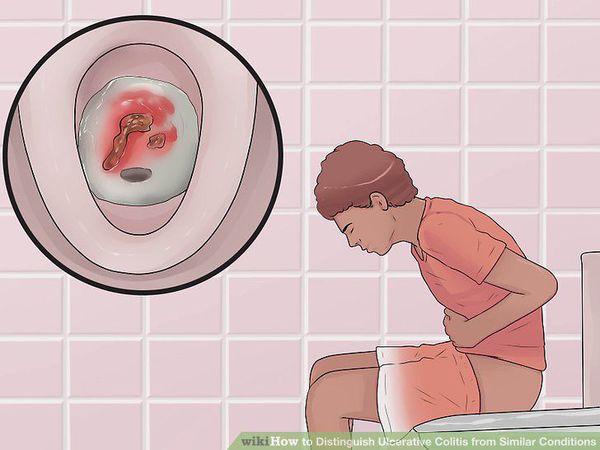
При поражении дистальных отделов толстого кишечника (проктит) чаще возникает запор, ложные позывы на дефекацию, тенезмы, в кале обнаруживаются следы алой крови, слизи или гноя. Для оценки тяжести язвенного колита предложены критерии Truelove и Witts.
При язвенном колите происходит каскад воспалительных реакций. В результате воздействия триггерного (инициирующего) фактора стимулируются Т- и В-лимфоциты, что, в свою очередь, приводит к образованию иммуноглобулинов М и G. Дефицит Т-супрессоров усиливает аутоиммунный ответ. Образование иммуноглобулинов М и G приводит к появлению иммунных комплексов и активации сиcтемы комплемента, который обладает цитотоксическим действием. В очаг воспаления проникают нейтрофилы и фагоциты, при этом высвобождаются медиаторы воспаления.
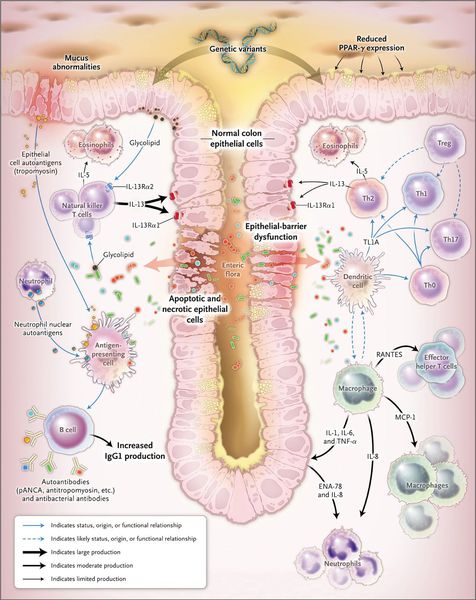
Одним из механизмов патогенеза язвенного колита является нарушение барьерной функции слизистой оболочки толстой кишки и регенераторной функции.
Реакция организма на стресс с патологическим нейрогуморальным ответом приводит к активизации аутоиммунного процесса. Часто больные язвенным колитом имеют эмоциональную нестабильность.
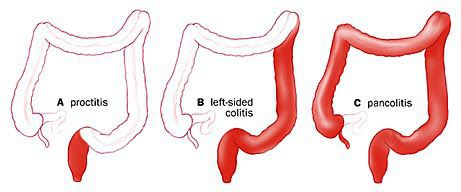
По распространённости процесса различают:
- проктит (с вовлечением прямой кишки);
- левосторонний колит (поражение прямой сигмовидной и нисходящей ободочной кишки);
- тотальный колит (поражение всех отделов толстого кишечника).
По степени тяжести течения:[3]
- лёгкое течение;
- среднетяжёлое течение;
- тяжёлое течение.
По характеру течения:
- острое течение (менее 6 месяцев от начала болезни);
- фульминантное (быстро развивающееся);
- постепенное;
- хроническое непрерывное течение (периоды ремиссии (ослабления симптомов) менее 6 месяцев при правильном лечении);
- хроническое рецидивирующее течение (периоды ремиссии более 6 месяцев): редко рецидивирующее (один раз в год или меньше) или часто рецидивирующее (более 2 раз в год).
Местные осложнения
К местным осложнениям относятся:
- перфорация;
- токсическая дилатация (расширение) толстого кишечника;
- обильное кишечное кровотечение;
- колоректальный рак.
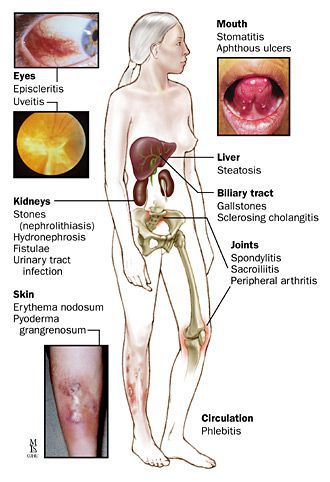
Системные осложнения
Проявляются внекишечными симптомами, причина которых до сих пор не изучена. Чаще поражаются ротовая полость, кожа, суставы.
К системным осложнениям относятся:
- узловатая эритема (поражение кожи и подкожной клетчатки);
- гангренозная пиодермия (поражение кожи крупными болезненными язвами);
- эписклерит (поражение эписклеральной ткани глаза);
- артропатия (поражение суставов);
- анкилозирующий спондилит (воспаление суставов позвоночника);
- поражения печени (повышение трансаминаз крови, гепатомегалия);
- первичный склерозирующий холангит (сужение просвета желчных протоков в результате воспаления).
При диагностике в первую очередь оценивается клиника заболевания, анамнез, производится осмотр с обязательным пальцевым исследованием прямой кишки.
Наиболее важными в диагностике язвенного колита являются эндоскопические методы исследования: ректороманоскопия, колоноскопия с биопсией. Так же для уточнения диагноза применяются ирригоскопия, МСКТ-колоноскопия.
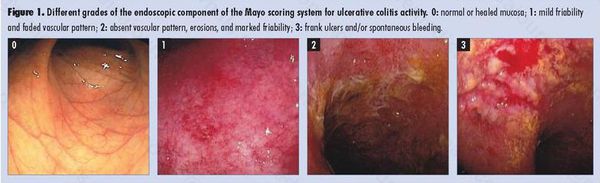
По эндоскопической картине можно определить степень воспаления толстого кишечника. Существуют четыре степени воспаления кишечника:
- При I степени наблюдается отёчность слизистой оболочки, гиперемия, сглаженность или отсутствие сосудистого рисунка, определяются точечные кровоизлияния, слизистая ранима, контактно кровоточит.
- При II степени добавляется зернистость, могут присутствовать эрозии, фиброзный налёт на стенках кишки.
- При III степени эрозии сливаются между собой, образуются язвы, в просвете кишки гной и кровь.
- При IV степени, помимо вышесказанного, появляются псевдополипы, состоящие из грануляционной ткани.
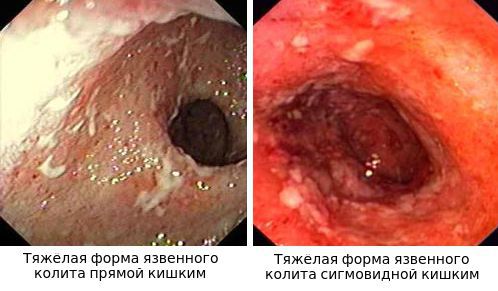
Язвы не проникают глубже подслизистого слоя.
При рентгенологическом исследовании определяется:
- отсутствие гаустр (мешкообразных выпячиваний стенки толстой кишки);
- сглаженность контуров;
- изъязвления, отёк, зубчатость, двойной контур;
- утолщение слизистой и подслизистой оболочек;
- преимущественно продольные и грубые поперечные складки;
- воспалительные полипы.
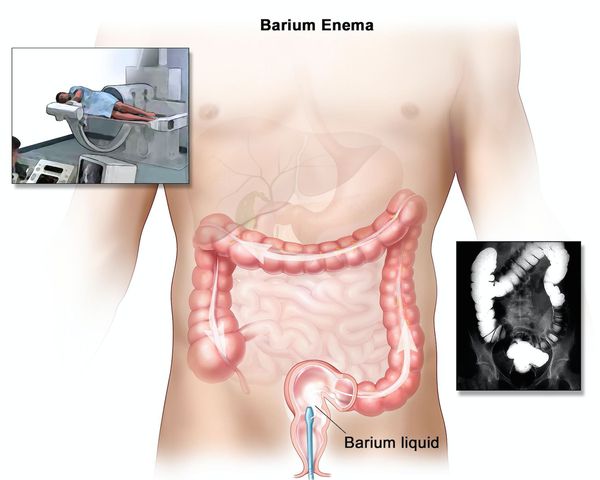
Ирригоскопия помогает не только в диагносте язвенного колита, но и в выявлении серьёзных осложнений, таких как токсическая дилатация (чрезмерное расширение просвета толстой кишки).
Дифференциальный диагноз:
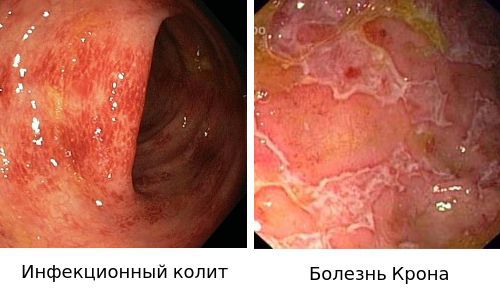
- Для подтверждения диагноза «Инфекционный колит» используют бактериологическое исследование.
- Диагноз «Болезнью Крона» ставится на основании эндоскопической картины и гистологического исследования биоптата слизистой.
- Ишемический колит.
Тактика зависит от локализации поражения и тяжести течения. При дистальных формах заболевания течение обычно лёгкое, поэтому больные могут лечиться в амбулаторных условиях. Тотальное или левостороннее поражение чаще имеет тяжёлое течение, поэтому требует госпитализации и лечения в условиях стационара.
Диета
Назначаются диеты № 4, 4Б, 4В по Певзнеру.
Консервативная терапия
К консервативной терапии относятся:
- аминосалицилаты, препараты 5-аминосалициловой кислоты (5-АСК, месалазин);
- кортикостероиды;
- иммунодепрессанты;
- билогическая терапия.
Аминосалицилаты являются препаратами первой линии и применяются в первую очередь. Для купирования атаки язвенного колита обычно требуется 3-6 недель терапии по 1-2 г/кг в сутки. После этого проводится противорецидивное лечение сульфасалазином (3 г/сут) или месалазином (2 г/сут).
При дистальном поражении (проктит) отдаётся предпочтение формам препарата в виде свечей. При левостороннем поражении — препаратам в форме пены для ректального применения. При тотальном поражении используют таблетированные формы препаратов.
При лечении данными препаратами ремиссия достигается в 74-81 % случаев.
Наиболее выраженным и эффективным противовоспалительным средством являются глюкокортикоиды.
Основными показаниями для лечения глюкокортикоидами являются:
- острое течение тяжёлой и среднетяжёлой степени;
- тяжёлое или среднетяжёлое левостороннее и тотальное поражение при наличии III степени воспаления по данным эндоскопического исследования;
- неэффективность или недостаточная эффективность лечения аминосалицилатами при хроническом течении заболевания.
При остром тяжёлом течении назначают внутривенное введение глюкокортикоидов (преднизолона не менее 120 мг/сут) 4-6 раз в день. Обязательно проводится коррекция водно-электролитного баланса, переливание компонентов крови, гемосорбция. Через неделю после внутривенного введения переходят на приём преднизолона внутрь. За это время проводится гастроскопия для исключения язвенной болезни желудка и двенадцатиперстной кишки.
При среднетяжёлой форме можно ограничиться пероральным приёмом преднизолона. Обычно преднизолон назначается в дозе 1,5-2 мг/кг массы тела в сутки. Максимальная доза 100 мг (у лиц пожилого возраста 60 мг).
Если отсутствуют побочные эффекты, то приём продолжают ещё 10-14 дней, затем снижают дозу на 10 мг каждые 10 дней. С 30-40 мг переходят на однократный приём преднизолона. С 30 мг дозу снижают по 5 мг в неделю. Обычно курс гормональной терапии составляет от 8 до 12 недель. Параллельно с гормонотерапией применяют аминосалицилаты до полной отмены гормонов.
При проктите применяются глюкокортикоиды ректально в микроклизмах. Обычно для этого используют гидрокортизон, применяют после дефекации 2 раза в день.
Побочные эффекты гормонотерапии:
- отёки;
- артериальная гипертензия;
- остеопороз;
- различные вегетативные расстройства;
- может способствовать развитию язвы желудка, а, как следствие, может возникнуть желудочно-кишечное кровотечение.
Современным глюкокортикоидом является буденофальк (содержащий будесонид). Суточная доза составляет 3 мг будесонида (1 капсула) 4-6 раз в сутки.
При лечении глюкокортикоидами может возникнуть гормональная зависимость или даже гормонорезистентность, которая формируется у 20-35 % больных тяжёлым язвенным колитом. Гормональная зависимость — это ответ организма на лечение глюкокортикоидами, при котором возобновляется воспалительный процесс после снижения дозировки.
При отсутствии эффекта от гормональной терапии назначают препараты, обладающие иммуносупрессивным действием, а также биологическую терапию. Основными из них являются 6-меркаптопурин и азатиоприн — это препараты первой линии. Они помогают уменьшить дозу гормонов и отменить их в 62-71 % случаев. Лечение обычно начинают вместе с гормонотерапией. Максимальная суточная доза — 150 мг. Незначительное количество побочных эффектов, по сравнению с глюкокортикоидами, позволяет применять препарат на протяжении многих лет.
Также существует аналогичный препарат — метотрексат, который применяется при непереносимости азатиоприна или для ускорения лечебного эффекта. Внутрь или внутримышечно по 30 мг в неделю. Эффект наступает через 2-4 недели
Если отсутствует эффект от азатиоприна и 6-меркаптопурина, применяют препараты второй линии — это инфликсимаб и циклоспорин А.
При отсутствии эффекта от второго введения инфликсимаба и 7-дневного курса циклоспорина А показано хирургическое лечение.
Противорецидивное лечение
После купирования острых воспалительных процессов, назначают противорецидивную терапию аминосалицилатами на срок до 6 месяцев. В случае успешного лечения и отсутствии клинических и эндоскопических признаков заболевания, терапию отменяют.
В случае нестабильного эффекта от противорецидивного лечения терапию продлевают дополнительно сроком на 6 месяцев.
При неэффективности монотерапии аминосалицилатами добовляют к лечению иммуносупрессоры (азатиоприн или 6-меркаптопурин) и гормоны.
Пациентам с язвенным колитом, получающих консервативную терапию, необходимо постоянное наблюдение врача, регулярное эндоскопическое исследование с биопсией.
Хирургическое лечение
По статистике хирургическое лечение показано больным в 11-22 % случаев. Единственным способом радикального хирургического лечения язвенного колита является колпроктэктомия, то есть удаление всей толстой кишки. Основными показаниями к хирургическому лечению являются:
- отсутствие эффекта от консервативного лечения;
- развитие осложнений язвенного колита (кровотечение, перфорация, рак, токсическая дилатация толстого кишечника).
Послеоперационные осложнения
Возникают у ослабленных пациентов на фоне тяжёлого течения заболевания:
- эвентрация (выпадение кишечника через дефект в брюшной стенке );
- несостоятельность швов кишечных стом;
- серозный перитонит (воспаление брюшины);
- полисерозит;
- абсцессы брюшной полости;
- пневмония.
При несвоевременном хирургическом лечении в послеоперационном периоде присоединяются другие осложнения в 59-81 % случаев, а летальность составляет от 11 до 49 %. При хирургическом лечении до возникновения тяжёлых кишечных осложнений (перфорация, токсическая дилатация и т. д.) эти цифры снижаются до 8-12 % и 0,5-1,5 % соответственно.
Таким образом, правильная диагностика, рациональная консервативная терапия и своевременное хирургическое лечение помогают добиться хороших результатов. В таком случае прогноз благоприятный. Но, в связи с длительным периодом нетрудоспособности, многие пациенты нуждаются в медико-социальной экспертизе и оформлении инвалидности.
Источник


