Лучевой колит прямой кишки
Лучевая терапия при злокачественных заболеваниях применяется с целью замедления роста опухоли, исключения развития метастазов. Процедура позволяет достичь положительного результата и улучшить прогноз. Но лучевая терапия может нанести серьезный вред здоровью. Одним из последствий является постлучевой колит.
Что такое
Колит характеризуется воспалением, которое поражает ободочную кишку. Причин развития заболевания может быть множество. Но одним из провоцирующих факторов считается лучевая терапия.
По теме
Заболевание возникает в случаях, когда воздействие радиоактивного излучения было направлено на органы малого таза, в область лимфатических узлов или гениталий.
Зачастую лучевой колит выявляется спустя несколько месяцев или лет после облучения. Специалистами установлено, что заболевание способно проявлять себя даже через 2 года. Именно поэтому пациентам требуется на протяжении данного срока регулярно посещать гастроэнтеролога.
Причины
Лучевой колит возникает в результате воздействия радиоактивного излучения при проведении курса лечения в случае выявления злокачественных образований.
Раковые опухоли могут поражать простату, мочевой пузырь, почки и органы репродуктивной системы женщины.
В медицине, в зависимости от характера течения патологии, выделяют острый, подострый и хронический колит. Данные формы отличаются интенсивностью симптомов.
Кроме этого, при остром поражении все изменения обратимы. Подострое возникает через 6 недель или полгода. К хроническому постлучевому колиту относят заболевание, признаки которого проявились более чем через 6 месяцев. При этом возникающие процессы уже необратимы.
Клиническая картина
Особенностью постлучевого колита является длительное отсутствие симптомов. По мере развития воспалительного процесса заболевание начинает маскироваться под другие болезни органов пищеварительной системы.
Основным проявлением считается дискомфорт, имеющий различную степень интенсивности. Зачастую он сопровождается болезненными ощущениями в области расположения очага. Они возникают на ранних стадиях только при физических нагрузках, в процессе дефекации.
По мере развития патологии возникают острые позывы к дефекации. Боли становятся постоянными, увеличивается их интенсивность. Характер схваткообразный.
По теме
В результате развития стриктур наблюдаются запоры. Из анального отверстия появляются выделения слизистого характер. Пациента может беспокоить диарея.
В каловых массах обнаруживается кровь, причиной которой становится внутреннее кровотечение. Позывы к дефекации болезненные, но кал отсутствует. В медицине подобный синдром носит название тенезма.
Постоянная диарея, чаще возникающая при тяжелых радиационных облучениях, приводит к обезвоживанию. Это обусловлено тем, что вместе с каловыми массами из организма выводятся минеральные вещества.
Внутренние кровотечения становятся причиной анемии. Данное состояние сопровождается слабостью, головными болями, головокружениями, снижением работоспособности.
Диагностика
Постановка точного диагноза вызывает затруднения, что обусловлено поздним проявлением признаков, которые схожи с другими заболеваниями ЖКТ.
После опроса пациента с целью определения степени поражения ободочной кишки назначаются методы инструментальной диагностики.
Эндоскопическое исследование
С помощью эндоскопа, на конце которого закреплены камера и осветительный прибор, специалист проводит визуальный осмотр внутренних органов, определяет степень распространения воспалительного процесса.
После эндоскопии возникает некоторый дискомфорт. Неприятные ощущения проходят спустя некоторое время после процедуры. Также может возникать отек слизистой, гиперемия и кровоточивость.
Рентгенологическое исследование
Рентген назначается для выявления наличия изменений на слизистой ободочной кишки, определения свищей и рубцов.
В некоторых случаях применяется контрастное вещество. Благодаря окрашиванию на снимке структур врачу удается определить наличие тканей, пораженных некрозом.
КТ или МРТ
Компьютерная и магнитно-резонансная томография является одним из самых информативных методов диагностики.
Послойное сканирование тканей позволяет исключить абсцессы, злокачественные поражения и скопление в брюшной полости жидкости.
В качестве дополнительных методов могут применяться дыхательные тесты. Они используются для выявления избыточного роста бактерий и непереносимости лактозы.
Лечение
При поражении тканей ободочной кишки радиоактивным излучением лечение осуществляется на основе степени распространения патологического процесса. В первую очередь пациентам назначают лекарственные средства, направленные на устранения воспаления, восстановление иммунитета. Также показано применение витаминов, пробиотиков.
По теме
С целью предотвращения кровотечения применяется аргоноплазменная коагуляция. Процедура предусматривает прижигание аргоном пораженных тканей.
В тяжелых случаях используется хирургическое вмешательство. Показанием к проведению операции является наличие спаек в просвете кишечника.
Питание
Лучевой колит негативно отражается на пищеварении. С целью улучшения моторики кишечника и предотвращения диареи или запора пациентам рекомендовано соблюдение диеты.
В первую очередь следует выпивать не менее 3 литров жидкости в сутки. Из рациона нужно исключить молочные продукты, жирные, жареные, соленые, копченые блюда. Запрещены маринады и консерванты.
Не следует употреблять шоколад, орехи. Рекомендуется полностью исключить напитки, содержащие кофеин и алкоголь.
Питание должно быть сбалансированным. Блюда лучше отваривать, готовить на пару или запекать без масла.
Осложнения
Постлучевой колит при отсутствии терапии приводит к развитию опасных осложнений. У пациентов наблюдается развитие макроцитарной анемии, характеризующейся нехваткой витамина В12.
Также наблюдается гемералопия. Заболевание проявляется в виде резкого ухудшения зрения при слабом свете.
Воспалительный процесс с течением времени поражает большие участки тканей, становясь причиной рубцевания, непроходимости кишечника, перфорации стенок органа. Подобные состояния приводят к возникновению свищей, абсцессов.
Более чем у половины больных устанавливается язва, при которой патологический процесс поражает прямую кишку. Болезнь продолжительное время протекает без проявления признаков.
По теме
С течением времени состояние пациента ухудшается, возникает слабость, болезненные ощущения усиливаются, становятся постоянными.
Постлучевой колит опасен для организма пациента, так как способен проявлять себя спустя 2 года после проведения лучевой терапии. При этом воспалительный процесс затрагивает большие участки тканей.
Именно поэтому важно регулярно посещать специалиста и проходить профилактические осмотры после прохождения курса терапии. Это поможет своевременно выявить заболевание, начать лечение, исключить развитие серьезных осложнений.
Источник
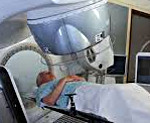
Лучевой энтероколит — это воспалительное поражение кишечника, связанное с радиационными воздействиями. Проявляется диареей, запорами, другими диспепсическими явлениями, патологическими примесями в кале, болями в животе, снижением веса, астенией. Диагностируется с помощью рентгеноконтрастного исследования тонкой, толстой кишки, колоноскопии, копрограммы, дыхательных тестов. Для лечения используют кортикостероиды, препараты 5-АМК, прокинетики, ингибиторы опиатных рецепторов, анионообменные смолы, антибиотики, пробиотики, ферментные средства, регенеранты в сочетании с диетотерапией. Оперативное лечение проводится при возникновении хирургических осложнений.
Общие сведения
Впервые характерные изменения кишечника после проведенной радиотерапии злокачественного новообразования были описаны в 1917 г. К.Францем и Дж.Ортом. По мере расширения показаний к проведению лучевой терапии, как радикального и паллиативного метода лечения онкологических заболеваний, совершенствования применяемых методик, число пациентов, получающих радиотерапию, увеличилось до 60% всех онкобольных. По результатам наблюдений специалистов в сфере практической проктологии, гастроэнтерологии и онкологии, у 3-17% больных, получивших радиационную нагрузку, развиваются ранние (острые) и поздние (хронические) формы лучевого энтероколита. Неятрогенное повреждение кишечника ионизирующими излучениями в настоящее время фиксируется крайне редко.
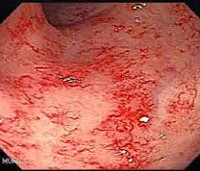
Лучевой энтероколит
Причины лучевого энтероколита
Пострадиационное воспаление кишечника обычно развивается у пациентов, принимающих радиотерапию по поводу злокачественных новообразований брюшной полости, забрюшинного пространства, малого таза. Прямое повреждающее воздействие на различные участки тонкой и толстой кишки возникает вследствие лучевого лечения рака желудка, поджелудочной железы, шейки матки, яичников, предстательной железы, яичек, мочевого пузыря, прямой кишки, почечных карцином, опухолей надпочечников, ретроперитонеальных лимфом и пораженных метастазами лимфоузлов. Радиационная толерантность тонкого кишечника достигает 35 Гр, толстого — 40 Гр. При более высокой лучевой нагрузке наступают отсроченные патологические изменения. Острая обратимая реакция в процессе терапии ионизирующим излучением может развиться и при меньших дозах.
Вероятность возникновения радиационного энтероколита повышается при наличии воспалительных заболеваний кишечника, послеоперационных спаек, ограничивающих подвижность петель тонкой кишки, у лиц пожилого возраста, пациентов, которым назначена химиотерапия. Дополнительными факторами риска являются сопутствующие заболевания (артериальная гипертензия, сахарный диабет), астеническое телосложение, использование устаревшей радиационной техники, неправильный расчет лучевой нагрузки, несоблюдение техники облучения. Развитие клиники радиационного энтероколита возможно в рамках острой лучевой болезни при равномерном внешнем облучении дозой более 20 Гр во время ядерных катастроф, при халатном отношении к технике безопасности во время работы с источниками ионизирующих излучений.
Патогенез
Механизм развития лучевого энтероколита зависит от времени возникновения заболевания. Раннее радиационное поражение, возникающее непосредственно в процессе радиотерапии или в течение первых трех месяцев после курса лечения, основано на цитотоксическом действии ионизирующего излучения. Десквамация, преходящая атрофия, гибель энтероцитов и колоноцитов сочетаются с неспецифической воспалительной реакцией. Укорочение ворсинок, отек, гиперемия, выраженная нейтрофильная инфильтрация собственной пластинки кишки нарушают пристеночное пищеварение, процессы расщепления нутриентов, всасывания воды, усиливают или угнетают перистальтику кишечника. Благодаря быстрому делению оставшихся эпителиальных клеток слизистая кишки полностью восстанавливается, явления энтероколита купируются.
При сверхвысоких дозах лучевой нагрузки развиваются стойкие поздние поражения, обусловленные патоморфологическими изменениями мелких подслизистых сосудов. Нарушение кровообращения в кишечной стенке, вызванное микротромбированием и гиалинозом артериол, приводит к развитию хронической ишемии и связанной с ней гипорегенераторной атрофии кишечных эпителиоцитов. При значительном истончении слизистой уплощается ее рельеф, повышается кишечная проницаемость, замедляется моторика, нарушается абсорбция основных питательных веществ, желчных кислот, возникают участки язв и эрозий, в тяжелых случаях происходит некротическая деструкция. Ситуацию усугубляет гипоксический реактивный фиброз мышечного слоя, осложняющийся рубцовым стенозированием просвета кишечника.
Классификация
Систематизация форм лучевого энтероколита учитывает время возникновения расстройства, выраженность и локализацию патоморфологических изменений кишечной стенки. Такой подход позволяет более точно спрогнозировать исход и подобрать адекватное лечение. Выделяют следующие варианты лучевого повреждения кишечника:
- По времени возникновения: ранние и поздние поражения кишечника. Острые формы лучевого воспаления возникают во время курса радиотерапии или на протяжении 3 месяцев после завершения лечения. В большинстве случаев они полностью обратимы. Для позднего лучевого повреждения, развивающегося спустя 4 и более месяцев после облучения, характерны хроническое течение, выраженные деструктивные изменения кишечника, менее благоприятный прогноз.
- По характеру патологических изменений: при оценке варианта энтероколита учитывается глубина повреждения кишечной стенки. Наиболее легкой формой является поверхностное катаральное воспаление. Для эрозивно-десквамативного и инфильтративно-язвенного лучевого воспалительного процесса, часто осложняющегося кишечными кровотечениями, характерен дефект слизистой вследствие полной атрофии эпителиоцитов. Самым тяжелым считается некротическое воспаление.
- По локализации воспаления: радиационный энтерит, колит. Хотя тонкая кишка более чувствительна к лучевой нагрузке, благодаря высокой мобильности она реже подвергается повреждению. Однако энтериты протекают тяжелее, чем колиты, и соответственно имеют более серьезный прогноз. При воспалении толстой кишки чаще возникают осложнения, требующие хирургического лечения. Заболевание протекает более тяжело при поражении обоих отделов кишечника.
Симптомы лучевого энтероколита
Клиническая картина острой формы заболевания сходна с признаками кишечного воспаления инфекционной этиологии. У пациентов наблюдается тошнота и рвота, потеря аппетита, учащенный стул с примесями слизи, боли в животе различной локализации. Значительное нарушение всасывания жиров проявляется выделением зловонных каловых масс светлого цвета с жирным блеском. При прогрессировании лучевой воспалительной реакции боли усиливаются, могут присоединяться ложные болезненные позывы к дефекации, в кале появляется кровь. Поздние радиационные энтероколиты характеризуются дискомфортом и умеренными болями в левой подвздошной области, других участках живота, чередованием запоров и диареи, потерей массы тела. Отмечаются нарушения общего состояния — головные боли, головокружения, слабость, снижение трудоспособности.
Осложнения
При язвенно-некротическом варианте лучевого энтероколита возникают потери крови с калом, которые со временем провоцируют формирование тяжелой железодефицитной анемии. Иногда развиваются профузные кровотечения, представляющие опасность для жизни больного. При лучевом энтероколите может происходить некроз всех слоев кишечной стенки, что приводит к перфорации и развитию местного или разлитого перитонита.
В случае хронического течения заболевания формируются рубцовые стриктуры, которые могут осложняться динамической или механической кишечной непроходимостью. Нарушение всасывания витаминов группы В сопровождается возникновением В12-дефицитной анемии, периферической полинейропатии. Ретиноловая недостаточность проявляется нарушением сумеречного зрения, слепотой, сухостью кожи и слизистых. При значительном недостатке эргокальциферола возможны остеопороз, кариес.
Диагностика
Постановка диагноза лучевого энтероколита не представляет затруднений при наличии в анамнезе сведений о радиационных воздействиях. Диагностический поиск направлен на тщательное обследование органов пищеварения с целью исключения других причин поражения кишечника. Наиболее информативными являются следующие инструментальные и лабораторные исследования:
- Рентгенологические методы. Рентгенография тонкого кишечника и ирригоскопия визуализируют признаки, характерные для лучевого поражения. Выявляются отсутствие гаустраций, сглаженность крипт слизистой, наличие язв или свищей, рубцовое сужение кишки. В сложных случаях выполняется МСКТ, МРТ брюшной полости.
- Колоноскопия. Введение эндоскопа через прямую кишку позволяет врачу осмотреть весь толстый кишечник. При энтероколите обнаруживаются очаги катарального воспаления слизистой, язвенные дефекты, точечные кровоизлияния, участки атрофии. Дополнительно выполняет биопсия кишечной стенки для гистологического анализа.
- Копрограмма. При анализе кала определяются типичные признаки лучевого воспаления: слизь, большое количество эритроцитов и лейкоцитов, примеси нейтральных жиров, непереваренных частиц пищи. Диагностика может дополняться бактериологическим посевом, который используется для выявления патогенной микрофлоры.
При хроническом воспалении с помощью мезентериальной ангиографии определяется поражение артериол, приводящее к ишемии. Для исключения других возможных причин энтероколита (непереносимости лактозы, СИБР) применяют функциональные Н2-дыхательные тесты. Для лучевого энтероколитического синдрома типично снижение количества гемоглобина и эритроцитов, микроцитоз, уменьшение содержания ретикулоцитов в клиническом анализе крови.
Дифференциальная диагностика проводится с воспалительными заболеваниями кишечника (терминальным илеитом, неспецифическим язвенным колитом), энтероколитами вирусной или бактериальной этиологии, амебиазом, целиакией, спру, первичной лактазной недостаточностью, синдромом избыточного бактериального роста (СИБР), злокачественными новообразованиями пищеварительного тракта. Кроме наблюдения у врача-проктолога или гастроэнтеролога, пациенту может потребоваться консультация онколога, радиолога, инфекциониста, гематолога, общего хирурга.
Лечение лучевого энтероколита
Терапевтическая тактика в целом напоминает схему ведения пациентов с болезнью Крона, язвенным колитом. Независимо от варианта энтероколитического лучевого синдрома, проводится коррекция питания. Больным рекомендован рацион с высоким содержанием белка (100-120 г/сут.), достаточным количеством углеводов, жиров, макро- и микроэлементов, витаминов. При тяжело протекающих поздних энтероколитах возможен перевод пациента на энтерально-зондовое и парентеральное питание. При умеренно выраженной симптоматике достаточным оказывается симптоматическое лечение. Пострадиационную диарею эффективно купируют анионообменные смолы и блокаторы опиоидных рецепторов.
Для стимуляции моторики применяют прокинетики, которые для редукции возросшего количества микроорганизмов комбинируют с нитроимидазолами и тетрациклинами. Слабительные могут назначаться при отсутствии кишечной обструкции. Чтобы стимулировать восстановление эпителия, используют нестероидные анаболики, регенеранты и репаранты. Назначение антагонистов H2-рецепторов или ингибиторов протонной помпы позволяет ускорить заживление участков с эрозиями и язвами. При нарушении процессов пищеварения показаны ферментные препараты. Для профилактика возможного дисбиоза используются пробиотики. При среднетяжелом и тяжелом течении оправдано проведение патогенетической медикаментозной терапии, включающей:
- Кортикостероиды. Противовоспалительная терапия глюкокортикоидами позволяет блокировать образование арахидоновой кислоты и некоторых других медиаторов воспаления, затормозить пролиферацию Т-хелперов, уменьшить содержание в крови моноцитов и за счет этого сократить количество тканевых макрофагов. Пациентам с энтероколитом обычно назначают прием преднизолона или метилпреднизолона.
- Производные 5-аминосалициловой кислоты. Их эффект основан на блокировании циклооксигеназного и липооксигеназного механизмов образования медиаторов воспаления — простагландинов, тромбоксанов, лейкотриенов. Лекарственные средства с 5-АСК угнетают продукции миофибробластами белка, тормозящего разрушение рубцовой ткани, что позволяет замедлить или предотвратить возникновение фиброза.
Терапевтическую резистентность тяжелого энтероколита позволяет снизить проведение гипербарической оксигенации. До 20-30% пациентов с поздним радиационным воспалением, выраженными стриктурами и стенозом нуждаются в оперативном лечении. В зависимости от ситуации проводятся сегментарная резекция тонкой кишки, энтероэнтеростомия, энтероколостомия, энтеростомия (еюностомия или илеостомия), резекции ободочной кишки, стомирование толстого кишечника, наложение различных типов толстокишечных анастомозов.
Прогноз и профилактика
У большинства больных с острым воспалением наблюдается полное выздоровление с восстановлением целостности слизистой оболочки. У 70-80% пациентов с хроническим процессом удается добиться стойкой клинической ремиссии консервативными методами. Прогностически неблагоприятной является язвенно-некротическая форма лучевого энтероколита, которая может приводить к серьезным осложнениям и ограничению трудоспособности пациентов. Профилактика радиационных поражений кишечника заключается в индивидуальном подборе курсовой и разовой дозы облучения, соблюдении перерывов между сеансами лучевой терапии, применении радиопротекторов.
Источник


