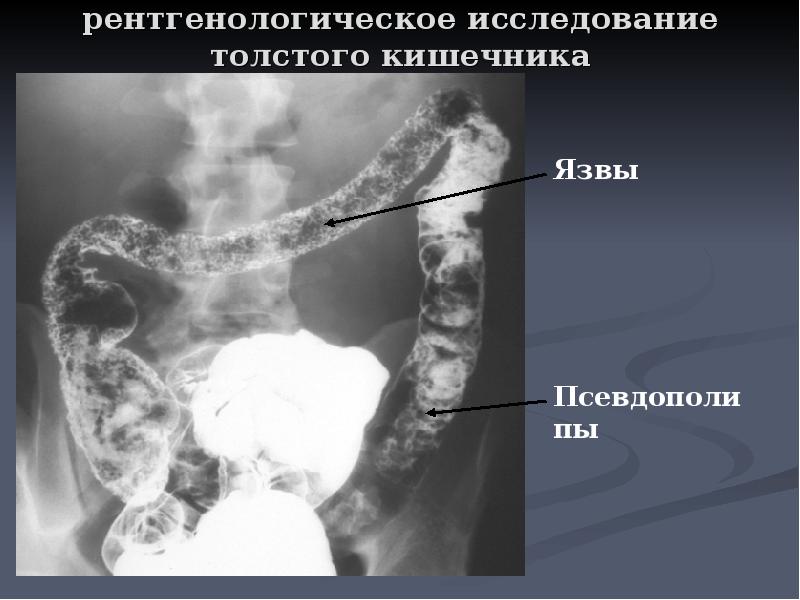
Обследование при неспецифическом язвенном колите

Колики в кишечнике
Неспецифический язвенный колит – это болезнь, характеризующаяся изменениями слизистой оболочки толстого кишечника. Воспаление наблюдается в нижней части толстой кишки, затрагивая прямую кишку тоже. Недуг протекает в постоянной или рецидивирующей формах. Чтобы поставить точный диагноз, необходима диагностика неспецифического язвенного колита, включающая проверенные и современные методы исследования.
Жалобы больного
Это основной метод диагностики. Самые распространенные признаки недуга заключаются в частом стуле до 20 раз в день, но в особых тяжелых случаях в каловых массах присутствует кровь. Часто человек обращается за помощью к врачу с кровотечением, болезненными ощущениями во время дефекации, острыми коликами в животе, общей слабостью, рвотой и температурой тела до 40 градусов.
Осмотр врачом
В зависимости от стадии развития болезни, возможны проявления сухости кожи и языка из-за обезвоживания организма. Пациент при пальпации области живота врачом может почувствовать резкие боли, доходящие иногда до перитонита, представляющего собой напряжения брюшной части из-за воспаления. Это свидетельствует про появление дыр в стенках толстого кишечника. Хороший результат дает пальцевой осмотр прямой кишки, позволяющий найти все гнойные образования в стенке прямой кишки, свищи, трещинки, уплотнения или бугристость прямой кишки. Этот способ поможет обнаружить наличие крови, гноя и слизи.
Анализы
При язвенном колите диагностика в лаборатории предполагает обследование больного, которому придется сдать:
- Общий анализ крови. Такой стандартный анализ позволит найти воспалительный процесс, для которого характерно увеличение уровня лейкоцитов в крови. Этот показатель составляет 9,0*10 в 9 степени/л. Также наблюдается повышение СОЭ, но при внутреннем кровотечении уровень гемоглобина наоборот понижается, в зависимости от количества потерянной крови.
- Анализ кала. Обследование способно определить наличие скрытой крови в каловых массах;
Биохимический анализ крови. Повышение в организме С-реактивного белка и понижение общего белка показывает на воспаление. По статистике, в 60% пациентов обнаруживают антинейтрофильные цитоплазматические антитела. Эти микроорганизмы действую против нейтрофилов, которые имеют свойство атаковать и становятся причиной развития воспаления. - Микробиологическое исследование. Пациент должен сдать посевы, которые берутся со слизистой, чтобы исключить инфекционную форму недуга. Организм проверяется на наличие патогенной флоры, на разные типы вирусов, хламидии, гельминты.
Колоноскопия или эндоскопический осмотр толстой кишки
Процедура проводится с гистологическим исследованием и биопсией. Этот метод точно определит неспецифический недуг. Исследование на клеточном уровне проводится, чтобы поставить более точный диагноз, ведь существует схожесть язвенного колита и болезни Крона из-за аналогичной эндоскопической картины. При колоноскопии появляется покраснение и отечность слизистой сигмовидной и толстой кишки, а также остальных областей толстого кишечника. Исследование сглаживает выпячивание наподобие ребер в прямой кишке, делая ее гофрированной.
Эндоскопия помогает обнаружить язвенные образования разного размера в слизистой оболочке в зависимости от стадии поражения или участки с кровотечениями. Такие дефекты часто находятся при средней и высшей тяжести протекания болезни. Язвы отличаются разными размерами, а дно их иногда покрывается фибрином или гнойными выделениями.
При средней стадии язвенного колита язвенные образования могут отсутствовать, хотя слизистая будет отмечаться рисунком в виде мелкого зерна. Если исследование показало наличие лишь одной язвы, то это может свидетельствовать о раке кишечника, хотя не нужно ранее срока паниковать. В этом случае, врач берет кусочек ткани из обнаруженного дефекта на биопсию и дальнейшую диагностику. Колоноскопия поможет определить тяжесть и длительность развития болезни.
Магнитно-резонансная томография

Аппарат МРТ
МРТ позволяет проверить любой больной орган на клеточном уровне. Способ диагностики основывается на способности ядер атомов реагировать на электромагнитные волны. Часто во время проведения процедуры используется контраст для более качественной диагностики няк. Жидкость состоит из жировой эмульсии с гадолинием или оксидов железа. Чтобы снизить перистальтику кишечника применяются спазмолитики, которые вводятся внутривенно или добавляются в выпиваемую воду. Это способствует улучшению проведения процедуры обследования слизистой.
Для более результативного осмотра используется искусственное вздутие кишечника с помощью ректальной клизмы или введения контраста пероральным способом. Чтобы снизить всасывание средства в организм пациента, применяются специальный составы для замедления этого процесса. Проведение такого метода диагностики не рекомендуется людям, страдающим клаустрофобией, эпилептическими и судорожными припадками. Перед процедурой врач должен быть осведомлен о наличии аллергических реакций на применяемый раствор, пластырей на теле или татуировок.
Рентген
Такой вид диагностики определяет токсический мегаколон. Это расширение толстого кишки, которое может угрожать жизни человека. Рентгенологическое исследование помогает обнаружить скопление газов в поперечном отделе кишечника или в брюшной полости, что свидетельствует о перфорации язвенной болезни. Отмечается исчезновение гаустр и неравномерность рисунка из-за развития язвенных образований. При затянувшейся болезни тяжелой формы просвет толстой кишки значительно сужается, а стенки кишечника отличаются повышенной жесткостью. Обострение недуга укорачивает толстую кишку из-за воспалительного процесса в организме человека.
Патоморфологическая диагностика
Исследование способно выявить, какую стадию развития имеет неспецифический недуг за счет симптоматики, осмотра и жалоб пациента:
- Легкая стадия подразумевает отечность и воспалительный процесс слизистой оболочки.
- Средняя степень отмечается воспалением, развитием язвенных дефектов и небольшого кровотечения.
- Тяжелая форма недуга представляет собой множественное появление язвенных образований, которые приводят к сглаживанию и потере рельефности слизистой. Из-за активного процесса восстановления возникают псевдополипы. Часто эта фаза обусловлена повышенным риском развития токсикоза, который становится причиной воспаления брюшной области и вздутия живота. При таких симптомах другой вид диагностики противопоказан.
Ирригоскопия

Снимок после ирригоскопии
Такой вид исследования проводится для получения полной информации о состоянии толстого кишечника, его рельефности и размера. Диагностика язвенного колита менее травматична, поэтому рекомендована пациентам, которым нельзя проводить колоноскопию по каким-либо причинам. После процедуры врач будет знать о состоянии стенок кишечника не только на прямых участках, но и на изгибах.
С помощью клизмы вводится контрастное вещество после предварительного очищения кишечника. Затем делается несколько снимков при изменении положения тела больного. После этого, толстая кишка опорожняется от контраста, позволяя изучить способность ее к сокращениям и рельеф. Если требуется более четкие рентгеновские снимки, то кишечник заполняется воздухом. Этот способ диагностики называется двойным контрастом. Вещество, оставшееся на стенках кишечника, помогает более детально рассмотреть его заднюю стенку.
Такое исследование не применяется у людей с большой длинной кишечника и у ослабленных больных. Также процедура запрещена при подозрении на кишечную непроходимость. Ирригоскопия подразумевает использование контраста на водорастворимой основе при угрозе перфорации стенок кишечника.
Ректороманоскопия
Дифференциальная диагностика проводится с помощью ректоскопа для обследования прямой и всех отделов сигмовидной кишки. Устройство для процедуры представляет собой жесткую трубку, длина которой достигает 30 см, а диаметр – 2 см. Прибор оснащен специальным аппаратом для подачи воздуха, осветителем и линзами. Благодаря исследованию врач способен увидеть состояние слизистой и найти такие новообразования как трещинки, опухоли, полипы, геморроидальные узлы, рубцы и пр. Если возникнет необходимость, то можно провести биопсию.
Ректороманоскопия не занимает много времени и проводится в больнице. Пациенту приходится снять всю одежду ниже пояса и принять коленно-локтевую позу или лечь на бок. Сначала врач исследует прямую кишку пальцами, после чего в анальное отверстие вводи ректоскоп на 5 см. Остальные манипуляции проводятся благодаря визуальному наблюдению, когда прибор продвигается лишь по каналу кишечника.
Гибкая сигмоскопия
Этот диагностический метод предполагает введение гибкого оптического аппарата с источником света на конце для исследования сигмовидной кишки. Процедура занимает всего лишь несколько минут. Такой осмотр не позволяет осмотреть более высокие отделы толстого кишечника. Сигмоскопия имеет небольшой риск перфорации толстой кишки.
УЗИ
Ультразвуковое исследование помогает быстро и эффективно установить расположение, установить размер и состояние кишечника при язвенном колите. Этот способ исследования полностью безопасен, позволяя применять его почти во всех направлениях медицины. В основном, процедура проводится при подозрении развития заболевания в брюшной части организма. Врачи советуют делать УЗИ кишечника для определения толщины стенок обследуемого органа, предотвращая возникновения разных недугов. Такое исследование незаменимо при динамическом наблюдении за пациентами с язвенным колитом, определяя действенность назначенной терапии.
Компьютерная томография
КТ часто называют виртуальной колоноскопией. Чтобы получить полную картину внутренней области толстого кишечника используются минимальные дозы рентгеновского облучения во время процедуры. Исследование занимает не более 20 минут и совершенно безболезненно. Этот метод диагностики поможет выявить утолщение стенки толстой кишки и неспецифический колит.
Во время процедуры больной ложится на специальный стол, а в анальное отверстие вводится трубка на глубину 5 см для подачи воздуха, позволяя расправить толстую кишку. Потом пациент помещается вместе со столом в рентгеновский аппарат. Во время работы прибор начинает вращаться по спирали, делая снимки с разных ракурсов. Что более качественного исследования применяется контрастный раствор на йодной основе. Жидкость вводится ректальной клизмой. Она не имеет свойства всасываться в кишечник, а окрашиванию поддается лишь слизистая органа.
Источник
Лабораторные
данные:
Общий анализ крови:
признаки анемии, лейкоцитоз со сдвигом
влево, увеличение СОЭ.Общий анализ мочи:
протеинурия умеренная.БАК: гипопротеинемия,
снижение содержания альбуминов,
увеличение Y-глобулинов, трансаминаз,
серомукоида, сиаловых кислот, фибрина.
4. Анализ кала: эритроциты, лейкоциты,
слизь в большом количестве.
Инструментальные
исследования:
Ректороманоскопия
и колоноскопия: в прямой кишке и других
отделах толстой кишки обнаруживается
отечность, гиперемия, зернистость
слизистой оболочки, ее кровоточивость,
эрозии и язвы, нередко покрытые гнойными
налетами.Ирригоскопия
(производится при хронической форме
заболевания в фазе затихания обострения):
сужение просвета кишки на пораженном
участке. Отсутствие или неравномерность
гаустр, при наличии глубоких язв — депо
бария.
Программа
обследования:
Общий анализ крови,
мочи, кала, бактериологическое
исследование кала, в том числе на
дизентерию.БАК: белок и белковые
фракции, трансаминазы, билирубин,
сиаловые кислоты, фибрин, серомукоид.Ректороманоскопия.
Колоноскопия.
Ирригоскопия.
Дифференциальный
диагноз
Прежде
всего, необходимо провести дифференциальный
диагноз с острой
дизентерией. В
связи с необходимостью соблюдения
противоэпидемического режима нередко
больной до установления правильного
диагноза обследуется в инфекционном
отделении. Дизентерию исключают на
основании отрицательных посевов кала
и исследований крови на антигены
дизентерийных бактерий. Эндоскопическая
картина, свойственная язвенному колиту
(см. выше), не характерна для дизентерии,
при которой, как правило, имеются лишь
гиперемия, эрозии и геморрагии. Важно
также, что антибактериальная терапия,
дающая быстрый эффект при дизентерии,
при неспецифическим язвенным колитом
или неэффективна или ведет к прогрессированию
болезни.
Дифференциально-диагностические
трудности возникают при болезни
Крона с
локализацией в прямой и ободочной кишке.
При язвенном колите в отличие от
гранулематозного отсутствуют поражения
перианальной зоны (свищи, трещины),
воспалительный процесс в кишке начинается
со слизистой оболочки и с самого начала
сопровождается кровотечениями,
отсутствует рельеф типа «булыжной
мостовой», щелевидные язвы. При
гистологическом исследовании биопсийного
или операционного материала в подслиэистом
слое отсутствуют характерные для болезни
Крона типичные эпителиоидные гранулемы
с клетками Пирогова—Лангханса.
Исключительно
важное значение имеет дифференциальный
диагноз с эндофитно растущими опухолями
толстой кишки (рак,
лимфома), диффузным
семейным полипозом, в
распознавании которых решающее значение
имеют колонофиброскопия с множественной
повторной биопсией пораженных участков
кишки.
Для
ишемического поражения толстой кишки
характерны боль в левой половине живота,
запоры и выделения крови с калом.
Дифференциально-диагностическими
критериями могут служить сосудистый
шум над брюшным отделом аорты, отсутствие
симптомов интоксикации и диареи.
Консервативное
лечение НЯК основывается на следующих
принципах:
диетотерапия;
базисная терапия
препаратами 5-аминосалициловой кислоты
и/или глюкокортикоидами (системного и
местного действия);антибактериальные
средства;цитостатики
(иммунодепрессанты);иммуномодуляторы;
симптоматическая
(«сопровождающая») терапия.
Лечение
НЯК должно быть комплексным, обязательно
с тщательным соблюдением режима дня и
питания. Необходимы спокойные прогулки
на свежем воздухе. При значительном
нарушении общего состояния, лихорадке,
истощении, метаболических сдвигах и т.
д. режим должен быть постельным.
Лечение
В
последние годы выработаны новые стандарты
лечения НЯК благодаря введению строгих
критериев медицины, основанной на
доказательствах. В целом эти стандарты
базируются на результатах контролируемых
исследований, данных метаанализов,
однако в отношении некоторых препаратов
существуют еще рекомендации, которые
основаны лишь на нескольких контролируемых
или даже неконтролируемых исследованиях.
Эффективность лечения оценивается либо
по проценту ремиссии, либо как «Odds
ratio» (с 95% доверительным интервалом)
исследований или метаанализов, т.е.
соотношением вероятности терапевтической
эффективности.
В настоящее
время принята последовательная тактика
лечения НЯК. Лечение в период обострения
определяется степенью тяжести рецидива,
а терапия в период ремиссии определяется
выбором терапии во время обострения
заболевания.
Терапевтические
подходы в период обострения заболевания
определяются тяжестью клинических
проявлений. Для оценки активности НЯК
чаще используется так называемый индекс
Truelove, который включает оценку частоты
стула, наличие видимой крови в кале,
повышение температуры тела, анемию,
тахикардию и СОЭ (рис. 1).
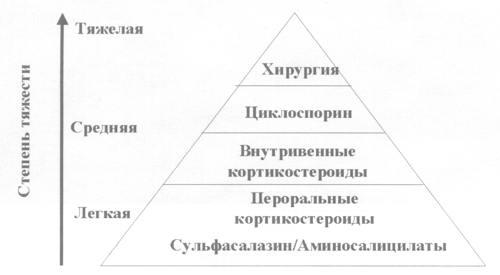
Так,
при легком и среднетяжелом обострении
назначаются аминосалицилаты, пероральные
кортикостероиды, в более тяжелых случаях
кортикостероиды назначаются внутривенно.
При неэффективности кортикостероидной
терапии возможно использование
циклоспорина. И последним этапом лечения
остается тотальная колэктомия.
Наиболее
широко для лечения обострения НЯК
продолжают использоваться аминосалицилаты
и кортикостероиды. Их эффективность
была доказана в многочисленных
плацебо-контролируемых исследованиях.
В 1930 г. д-р Swartz (Швеция), пытаясь создать
новый препарат для лечения ревматоидного
артрита и комбинируя салицилаты
(5-аминосалициловую кислоту) и сульфаниламид
(сульфапиридин), открыла салазосульфапиридин
(сульфасалазин). Первые результаты
лечения ревматоидного артрита были не
слишком впечатляющими, но затем она
применила этот препарат у больных
язвенным колитом в сочетании с поражением
суставов и получила грандиозные
результаты. Внедрение сульфасалазина
в лечение НЯК открыло новые возможности
терапии данного заболевания: была
найдена альтернатива глюкокортикоидам
и появилась возможность проведения
поддерживающей терапии.
В
одном из метаанализов было показано,
что при лечении дистальной формы НЯК
доказанно эффективны в сравнении с
плацебо назначаемые местно 5-аминосалицилаты.
Однако дозозависимый эффект доказан
не был, т.е. аминосалицилаты в дозе от
0,5 до 1,5 г в виде суппозиториев или от 1
до 4 г в виде клизм одинаково эффективны.
Другой метаанализ подтвердил, что
кортикостероиды эффективнее плацебо,
однако при сравнении местных
кортикостероидов с местным использованием
5-аминосалицилатов последние были
эффективнее. При тотальном поражении
толстой кишки аминосалицилаты в дозе
выше 3 г/сут также превзошли эффект
плацебо (рис. 2). Отмечена достоверно
более высокая эффективность сульфасалазина
по сравнению с месалазином в исследованиях
длительностью не более полугода, при
увеличении сроков исследования
достоверное различие утрачивалось,
однако тенденция сохранялась (рис. 3).
Хотя общепринято, что терапевтическим
эффектом обладает 5-аминосалициловая
кислота, результаты многочисленных
исследований показали, что собственно
сульфасалазин оказывает противовоспалительное
действие, отличающееся от 5-аминосалициловой
кислоты. Так, было установлено, что
сульфасалазин подавляет фосфолипазу
А, ключевой фермент каскада арахидоновой
кислоты, и блокирует рецепторы к фактору
некроза опухоли. Эти данные подтверждаются
клиническими наблюдениями значительно
более высокой эффективности сульфасалазина
по сравнению с 5-аминосалициловой
кислотой при лечении ревматоидного
артрита, в связи с этим при сочетании
хронических воспалительных заболеваний
кишечника с поражением суставов
рекомендуется использование сульфасалазина.
Значительную часть побочных эффектов
сульфасалазина, как токсических
(дозозависимых), так и аллергических
(дозонезависимых), приписывают
сульфокомпоненту. Только свободная,
несвязанная, метаболизированная
(глюкоронированная) форма сульфапиридина
способна вызывать побочные эффекты,
что в свою очередь связано со способностью
больного как ацетилятора. В группе
быстрых ацетиляторов дозозависимые
(токсические) побочные эффекты наблюдались
значительно чаще. Очень частые
нежелательные побочные эффекты, такие
как тошнота, рвота и головная боль, в
большинстве случаев исчезают после
уменьшения дозы. Однако развивающиеся
реже аллергогиперергические реакции
(например, агранулоцитоз, гемолитическая
анемия) требуют немедленной отмены
препарата.
Согласно последним
исследованиям начало терапии с малой
дозы 0,5 г/сут с постепенным подъемом
дозы в 3 раза в течение 4–6 дней значительно
снижает частоту вышеперечисленных
токсических побочных эффектов. Для
предотвращения аллергических реакций
предлагаются различные варианты
направленной десенсибилизирующей
терапии.
При тяжелых формах
НЯК целесообразно использование
кортикостероидов в дозе 40–60 мг
преднизолонового эквивалента в сутки
с постепенным снижением дозы 10–5 мг в
неделю после достижения клинического
эффекта. При отсутствии эффекта на
введение больших доз преднизолона в
течение 7–14 дней возможно применение
циклоспорина в дозе 4 мг на 1 кг массы
тела внутривенно с переходом через 3–7
дней на пероральный прием из расчета 5
мг/кг в сутки в течение 4–6 мес. Основанием
для продолжения лечения циклоспорином
в течение столь длительного срока после
достижения ремиссии служит ожидание
первого эффекта азатиоприна, применяемого
в качестве средства поддержания ремиссии.
Антибактериальное лечение и парентеральное
питание хотя и назначаются в тяжелых
случаях, эффективность этих мероприятий
не доказана.
Ремиссионная
терапия определяется выбором препаратов
для лечения острого процесса. Так, для
поддержания ремиссии после использования
местных и системных форм аминосалицилатов
переходят на поддерживающую дозу в той
же форме введения. Риск развития рецидива
доказанно снижается при постоянном
приеме поддерживающей дозы аминосалицилатов,
причем при дистальном колите более
эффективно местное введение. При
тотальном колите приблизительно
одинаково эффективны 5-аминосалицилаты
и сульфасалазин. После кортикостероидной
терапии возможно использование
аминосалицилатов в поддерживающей дозе
(0,75–2 г/сут), а также переход на цитостатики:
азатиоприн из расчета 2 мг на 1 кг массы
тела или 6-меркаптопурин. После циклоспорина
применяются только цитостатики. По
данным одного из исследований,
поддерживающая доза цитостатиков
позволяет избежать колэктомии в 66%
случаев, в то время как при сочетании с
5-АСК этот процент значительно ниже:
всего 40 (рис. 4). В большинстве случаев
резистентность к лечению обусловлена
слишком низкой дозировкой препаратов.
Необходимо применение только доз
препаратов, зарекомендовавших себя
эффективными в рамках исследований.
Рис.
1. Индекс активности НЯК (индекс Truelove).
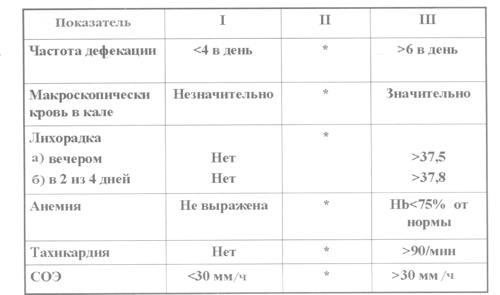
Рис.
5. Пирамида терапии при обострении НЯК.
Прогресс
в понимании патогенеза воспалительных
заболеваний кишечника привел к внедрению
новых препаратов, воздействующих на
иммунную систему и воспалительный
ответ. К таковым можно отнести инфликсимаб,
блокатор фактора некроза опухоли альфа.
Фактор некроза опухоли альфа относится
к ключевым цитокинам, принимающих
участие в развитие воспалительных
заболеваний кишечника. В отношении
эффективности инфликсимаба при лечении
НЯК не проведено ни одного крупного
рандомизированного контролируемого
исследования. Результаты одного
контролируемого и нескольких
неконтролируемых исследований
свидетельствуют, что инфликсимаб может
быть использован при лечении обострения
НЯК. Однако другое небольшое контролируемое
исследование подтвердило его
неэффективность при стероидорефрактерном
язвенном колите. Учитывая разнонаправленность
полученных результатов, планируется
проведение крупного плацебо-контролируемого
исследования.
К сожалению,
в случаях тяжелого, резистентного к
терапии тотального НЯК, а также при
развитии осложнений может потребоваться
проведение хирургического
вмешательства. Абсолютными
показаниями являются:
•
перфорация,
• кишечная
непроходимость,
• токсический
мегаколон,
• абсцесс,
•
кровотечение,
• высокая
степень дисплазии или рак толстой
кишки.
Относительными
служат:
•
неэффективность консервативной терапии
при выраженной активности,
•
задержка развития у детей и подростков,
•
фистулы,
• низкая степень
дисплазии эпителия.
Необходимость
хирургического лечения в течение жизни
возникает приблизительно у 20% больных,
что значительно ниже, чем при болезни
Крона, при которой вероятность
хирургического вмешательства в течение
20 лет заболевания достигает
90%.
Поучит
Стандартом
хирургического лечения при НЯК в
настоящее время служит тотальная
колэктомия с наложением поуч-анастомоза.
Воспаление данного искусственно
сформированного резервуара (поучит) в
течение первых двух лет после операции
развивается примерно у 30% больных.
Воспаление может принимать острый и
хронический характер. Последний
наблюдается приблизительно у 5% больных
поучитом. В качестве препаратов первого
выбора для лечения поучита применяются
антибиотики (метронидазол 400 мг 2–3 раза
в сутки или ципрофлоксацин 250–500 мг 2
раза в сутки) в течение 14 дней. При их
неэффективности может потребоваться
смена антибактериального препарата. В
отношении применения аминосалицилатов,
кортикостероидов и иммуносупрессоров
не существует данных исследований,
поэтому эти препараты могут быть
использованы только как индивидуальное
пробное лечение. Новейшие исследования
подтверждают эффективность при
хроническом поучите определенных
пробиотиков. При резистентных к терапии
формах поучита может потребоваться
экстирпация поуча с наложением стомы.
Диета
при НЯК
Относительно
эффективности назначения диеты при НЯК
на сегодняшний день пока не опубликовано
ни одного метаанализа, и современное
состояние проблемы можно оценить лишь
на основании рандомизированных
клинических исследований. Из 11
опубликованных исследований в 6
применялись ненасыщенные омега-3-жирные
кислоты или рыбий жир. В остальных
исследованиях оценивали эффективность
элиминационной диеты, дополнительного
питания, богатого балластными веществами.
Величина исследований достаточно
небольшая (11–105 больных), что зачастую
усложняло статистическую обработку
данных. Период наблюдения составлял от
7 мес до 1 года. По полученным данным,
назначение рыбьего жира не изменяет
естественное течение заболевания,
однако статистическая достоверность
ограничена размером исследований.
Однако в двух исследованиях было
достигнуто значимое снижение дозы
кортикостероидов и прибавка массы тела
при обострении заболевания.
Таким
образом, суммируя сказанное выше, схема
ведения больных НЯК выглядит как показано
на рис. 5.
Психосоциальные
аспекты
Традиционно
воспалительные заболевания кишечника
рассматривались как пример
«психосоматических» заболеваний,
что связано с тем, что больные и их
родственники часто связывают начало
заболевания или возникновение обострения
с пережитым стрессом или другими
психологическими факторами. Однако
нужно помнить, что данное предположение
не удалось подтвердить в ходе контролируемых
клинических исследований. По данным
исследований, нет типа личности, который
предрасполагал бы к развитию воспалительного
заболевания кишечника. Вполне понятно,
что у пациентов развиваются вторичные
изменения психики, связанные с зависимостью
от рецидивов, приема лекарственных
препаратов, посещений врача. Значимость
психотерапевтического лечения для
течения заболевания также не подтверждена.
Особое внимание необходимо уделить
социальной и профессиональной адаптации
пациента, что требует доверительных
отношений между врачом и больным.
Прогноз
С
момента внедрения в клиническую практику
кортикостероидов и сульфасалазина
статистика смертности от НЯК изменилась
коренным образом. До эры кортикостероидов
смертность при тяжелом обострении
превышала 30%, в настоящее время – менее
2%. В целом ожидаемая продолжительность
жизни при НЯК практически не отличается
от таковой в среднем в популяции (через
15 лет заболевания – 94,2%). Основными
причинами смерти помимо основного
заболевания остаются колоректальный
рак, бронхиальная астма и различные
патологии печени неалкогольной
этиологии.
Без проведения
поддерживающей терапии в ремиссионный
период примерно у половины больных
обострение возникает в течение двух
лет. Течение заболевания определяется
предшествующей воспалительной
активностью. Если в анамнезе отмечалось
частое рецидивирование, высока вероятность
быстрого возникновения рецидива. Если
ремиссия сохраняется в течение одного
года, риск рецидива составляет лишь
20%. Прогноз относительно активности
заболевания более благоприятен у
курящих. С течением времени частота и
степень тяжести обострения, как правило,
уменьшаются.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник