Терапия первой линии фульминантного язвенного колита включает
В статье рассмотрена роль системных и топических кортикостероидов в терапии язвенного колита
Язвенный колит (ЯК) представляет собой хроническое идиопатическое воспалительное заболевание с повреждением слизистой оболочки толстой кишки. При ЯК поражается только толстая кишка (за исключением ретроградного илеита), в процесс обязательно вовлекается прямая кишка, воспаление чаще всего ограничивается слизистой оболочкой (за исключением фульминантного колита) и носит диффузный характер. ЯК характеризуется периодами активного проявления симптомов заболевания, которые перемежаются периодами клинической ремиссии [1]. В 2012 г. статистический анализ показал, что в мире распространенность ЯК достигла 249 на 100 тыс. человек в Северной Америке и 505 на 100 тыс. человек в Европе; самые высокие годовые показатели заболеваемости ЯК были 19,2 на 100 тыс. человеко-лет в Северной Америке и 24,3 на 100 тыс. человеко-лет в Европе [2]. Самый высокий уровень заболеваемости, по-видимому, отмечается в возрасте 20–30 лет, хотя есть некоторые доказательства второго пика заболеваемости в более позднем возрасте [2]. Однако наличие второго пика заболеваемости признается не всеми специалистами, занимающимися воспалительными заболеваниями кишечника (ВЗК).
Эндоскопическое исследование толстой кишки у больных ЯК выявляет ряд характерных повреждений слизистой оболочки толстой кишки (СОТК): отсутствие сосудистого рисунка, гиперемию, зернистость, контактную кровоточивость, наличие эрозий и язв [1, 3]. В настоящее время заживление СОТК при ЯК рассматривается как одна из ключевых конечных точек в клинических исследованиях, а достижение заживления СОТК в клинической практике – как реальная возможность изменить течение ЯК и сохранить функции кишечника. В исследованиях последних лет показано, что заживление СО как при ЯК, так и при болезни Крона (БК) достоверно связано с большей продолжительностью клинической ремиссии заболевания, более низкой частотой рецидивов, более низким риском развития колоректального рака и более высоким качеством жизни [4, 5], а также существенно меньшей частотой кол-эктомий [6].
Существующие руководства по лечению взрослых больных ЯК в США [7], Европейском союзе [8] и Российской Федерации [9] рекомендуют в качестве первой линии терапии для индукции ремиссии у пациентов с легкой и среднетяжелой формами ЯК препараты 5-аминосалициловой кислоты (5-АСК). Такое лечение считается наиболее эффективным при комбинации системных и пероральных препаратов 5-АСК [7–9]. В случае неэффективности 5-АСК препаратами второй линии являются глюкокортикостероиды (ГКС) [7–9]. Однако ГКС I поколения, такие как преднизолон, имеют ряд побочных эффектов: повышенный риск развития инфекционных осложнений, остеопороза, синдрома Иценко – Кушинга, развитие стероидного диабета, симптоматической гипертензии и даже повышенный риск смертности по сравнению с таковым в общей популяции [7, 10–12].
В настоящее время для лечения ВЗК применяется несколько глюкокортикоидов топического действия для приема внутрь и для ректального введения: будесонид, тиксокортола пиволат, беклометазон, флютиказон [13]. В России с 2004 г. зарегистрирован и успешно применяется препарат Буденофальк (компания Dr. Falk, Германия) в форме капсул для приема внутрь. Одна капсула Буденофалька содержит 3 мг будесонида. При ряде заболеваний, например при бронхиальной астме и сезонном аллергическом рините, будесонид так же эффективен, как системные ГКС, отличаясь при этом лучшей переносимостью и меньшим влиянием на гипоталамо-гипофизарно-адреналовую систему. Это послужило основанием для применения будесонида при БК. Будесонид является первым топическим кортикостероидом, имеющим сродство к глюкокортикоидным рецепторам приблизительно в 8,5, 15 и 195 раз больше, чем у дексаметазона [14], преднизолона [15] и гидрокортизона [15] соответственно. Кроме того, будесонид почти не всасывается из кишечника, характеризуется низкой системной биодоступностью (не более 10% по сравнению с таковой преднизолона и гидрокортизона) и быстрым пресистемным метаболизмом. Последнее обеспечивает отсутствие токсичных метаболитов в крови после первого прохождения препарата через печень. Однако наиболее высокая внутрипросветная концентрация действующего вещества и, соответственно, наибольшая эффективность Буденофалька достигаются, начиная с терминального отдела подвздошной кишки и до поперечной ободочной кишки.
ЯК – это хроническое заболевание, поражающее только СОТК, сопровождающееся ее воспалением, отеком и образованием язвенных дефектов. Воспаление всегда начинается с прямой кишки, непрерывно распространяясь выше вплоть до поражения СО всех отделов толстой кишки. Таблетированный мультиматричный (ММХ) будесонид является представителем II поколения кортикостероидов, созданным для доставки активного вещества на протяжении всей толстой кишки. В фармакокинетических исследованиях среднее относительное всасывание будесонида в месте между восходящей кишкой и нисходящей/сигмовидной кишкой составило 95,9% (рис. 1) [16]. В 2-х похожих по дизайну исследованиях 3-й фазы (CORE I и II) однократный ежедневный прием будесонида ММХ 9 мг оказался эффективным и хорошо переносимым для индукции ремиссии ЯК легкой и средней степени тяжести. Частота клинической и эндоскопической ремиссии составила 17,9% (CORE I) и 17,4% (CORE II) для будесонида ММХ 9 мг по сравнению с плацебо 7,4% и 4,5% соответственно (p<0,05, будесонид ММХ 9 мг по сравнению с плацебо в обоих исследованиях), 12,1% с месалазином 2,4 г и 12,6% с будесонидом 9 мг, высвобождаемым в подвздошной кишке. По данным исследования поддерживающей терапии будесонидом в течение 12 мес., будесонид ММХ 6 мг может удлинять время до рецидива заболевания: среднее время составило 1 год для будесонида ММХ 6 мг по сравнению с 181 днем (р=0,02) для плацебо; однако необходимы дальнейшие исследования. В исследованиях CORE будесонид ММХ проявил хороший профиль безопасности; большинство нежелательных явлений (НЯ) были легкими или умеренными по своей интенсивности, серьезные НЯ были очень редкими. Более того, частота побочных реакций, возможно, связанных с глюкокортикоидами, была сравнима среди групп лечения. Долгосрочная безопасность (12 мес.) будесонида ММХ была сравнима с таковой плацебо. Эти данные подтверждают возможность включения ММХ будесонида в алгоритм лечения ЯК [17–20].
Будесонид ММХ для лечения и индукции ремиссии ЯК
Эффективность и безопасность будесонида ММХ для индукции ремиссии пациентов с легкой и умеренной активностью ЯК (индекс активности заболевания 4–10) изучались в похожих по дизайну рандомизированных исследованиях CORE I и CORE II [17–20]. В CORE I сравнивали будесонид ММХ 9 мг и 6 мг с месалазином 2,4 г и плацебо, тогда как в CORE II сравнивались те же дозы будесонида ММХ с будесонидом 9 мг, высвобождающимся в подвздошной кишке, и плацебо. В обоих исследованиях терапия проводилась 8 нед., и первичными точками были клиническая и эндоскопическая ремиссия на 8-й нед. лечения. Ремиссия определялась как индекс активности ЯК ≤ 1 со значением 0 для ректального кровотечения и частоты стула, отсутствие ранимости СО при колоноскопии, и снижение ≥ 1 эндоскопического индекса от исходного значения. В обоих исследованиях клиническая и эндоскопическая ремиссия была достигнута у значительной части пациентов, получавших будесонид ММХ 9 мг (по сравнению с плацебо). В исследовании CORE I ремиссия на 8-й нед. была достигнута у 17,9% пациентов, получавших будесонид ММХ 9 мг, у 7,4% (р=0,01) в группе плацебо и у 12,1% в группе, получавшей месалазин. В исследовании CORE II частота ремиссии к 8-й нед. составила 17,4% у пациентов, получавших будесонид ММХ 9 мг, по сравнению с 4,5% (p=0,005) и 12,6% (p=0,048) в группах, получавших плацебо и будесонид, высвобождающийся в подвздошной кишке, соответственно. Кроме этого, анализ подгруппы в исследовании CORE II показал, что при приеме будесонида ММХ 9 мг существенно большая часть пациентов с левосторонним ЯК достигла клинической и эндоскопической ремиссии, чем при приеме плацебо (17,7% по сравнению с 5,8% соответственно; p=0,03); часть пациентов с распространенным заболеванием, которые достигли клинической и эндоскопической ремиссии, также была больше при использовании будесонида ММХ 9 мг, чем при использовании плацебо (13,8% по сравнению с 0% соответственно), но это различие не было статистически значимым (p=0,10). В исследовании CORE I анализ подгрупп по тяжести заболевания показал, что у пациентов с легким течением ЯК (индекс активности ЯК 4 или 5), которые получали будесонид ММХ 9 мг или плацебо, клиническое улучшение (определялось как снижение ≥ 3 баллов индекса активности ЯК) было достигнуто у 44,4% и 25,0% пациентов соответственно; у пациентов с умеренной активностью заболевания (индекс ЯК ≥ 6 и ≤10) показатели клинического улучшения составили 39,7% и 30,1% соответственно. Более того, частота заживления СО была больше при применении будесонида MMX 9 мг, чем при применении плацебо, у пациентов с проктосигмоидитом (32,4% по сравнению с 19,5% соответственно; p=0,20) и левосторонним ЯК (40,6% по сравнению с 26,5% соответственно; p=0,22). Похожее различие в пользу будесонида ММХ 9 мг наблюдалось у пациентов с распространенным ЯК (16,1% по сравнению с 10,0% при применении плацебо), но это различие также не было статистически значимым (p=0,39). В анализе исследований CORE I и CORE II пациенты, получающие будесонид ММХ 9 мг, достигали клинической и эндоскопической ремиссии в 3 раза чаще, чем при получении плацебо [ОШ 3,3 (95% ДИ 1,7–6,4)]. Будесонид ММХ 9 мг был статистически значимо более эффективен по сравнению с плацебо у нескольких групп пациентов: мужского и женского пола ≤ 60 лет; ранее принимавших месалазин; не получавших месалазин ранее; с легким течением ЯК на исходном уровне; со средней тяжестью ЯК исходно; с проктосигмоидитом; с левосторонним ЯК; с длительностью ЯК ≥ 1 года и ≤5 лет; с длительностью ЯК > 5 лет.
Будесонид ММХ 9 мг для поддержания ремиссии ЯК
Эффективность будесонида ММХ 9 мг для поддержания ремиссии была изучена у пациентов, которые достигли клинической и эндоскопической ремиссии в исследованиях CORE I и CORE II, у пациентов в исследованиях CORE I и II, которые получали дополнительно 8 нед. лечения (будесонид ММХ 9 мг), и открытом исследовании, в котором пациенты были рандомизированы на группы, получавшие будесонид ММХ 6 мг или плацебо в течение 12 мес.; первичная точка эффективности – клиническая ремиссия, которая оценивалась через 1, 3, 6, 9 и 12 мес. Среднее время до рецидива заболевания (определялось как ректальное кровотечение, частота стула более чем 1–2 р./сут или оба этих фактора) составило 181 день в группе плацебо, но не было достигнуто в группе будесонида ММХ (p=0,02); к 12 мес. вероятность рецидива составила 59,7% и 40,9% соответственно. Однако процентное соотношение пациентов, у которых ремиссия поддерживалась в течение 12 мес., не различалось существенно между группами, что, возможно, связано со статистическими недостатками исследования.
Следовательно, польза будесонида ММХ в поддержании ремиссии в настоящее время недостаточно ясна, и необходимо проведение дальнейших исследований [21].
Побочные эффекты
В целом у молекулы будесонида более благоприятный профиль безопасности, чем у I поколения пероральных кортикостероидов, таких как преднизон или преднизолон. Например, в двойном слепом исследовании в течение 10 нед. 176 пациентов с БК, которые получали преднизолон по схеме снижения или будесонид, высвобождающийся в подвздошной кишке, в течение 10 нед., частота побочных явлений, связанных с глюкокортикоидами, была значительно ниже при применении будесонида, чем преднизолона (33% по сравнению с 55% соответственно; p=0,003). Кроме этого, подавление гипоталамо-гипофизарно-надпочечниковой системы, оцениваемое с помощью измерения средней концентрации кортизола в плазме, было существенно выше при применении преднизолона, чем будесонида, высвобождавшегося в подвздошной кишке, через 4 нед. (р<0,001) и 8 нед. (р=0,02). Благоприятный профиль НЯ будесонида ММХ у пациентов с ЯК был показан в исследованиях CORE I и II.Частота НЯ у пациентов, получающих будесонид ММХ 9 мг или 6 мг, составила 57,5% и 58,7% соответственно в исследовании CORE I, 55,5% и 62,5% соответственно – в CORE II. В обоих исследованиях большинство НЯ было легкими или умеренными по интенсивности, частота серьезных НЯ была ниже и схожей во всех группах лечения. Наиболее распространенными НЯ у пациентов, получавших будесонид ММХ, были головная боль, тошнота. В исследованиях CORE I и II частота НЯ, возможно, связанных с ГКС (акне, задержка жидкости, гиперемия, гирсутизм, инсомния, изменение настроения, «лунное» лицо, нарушение сна, образование стрий), была сравнима с таковой для будесонида ММХ 9 мг (10,2%), 6 мг (7,5 %) и плацебо (10,5%). Самыми распространенными НЯ, возможно, связанными с ГКС, при применении будесонида ММХ 9 мг по сравнению с плацебо были изменения настроения (3,5% и 4,3% соответственно) и нарушение сна (2,7% и 4,7% соответственно). В исследовании будесонида ММХ 6 мг в течение 1 года профиль безопасности был сравним с таковым плацебо [22].
Клиническое наблюдение
Больной Б., 22 года. Болен с 2013 г., диагноз «язвенный колит» поставлен при колоноскопии в ГНЦ колопроктологии и подтвержден гистологически в 2013 г. Принимал постоянно месалазин 3 г/сут. Амбулаторно проведена колоноскопия 24.11.2014 г.: язвенный колит, тотальное поражение, минимальная активность. С января 2016 г. отменил прием препаратов 5-АСК. В феврале 2016 г. отметил появление примеси крови в стуле. Возобновил прием месалазина 3 г/сут со слабоположительным эффектом, кровь в стуле сохранялась.
Однако с середины марта 2016 г. состояние ухудшилось, кроме примеси крови в стуле отмечались диарея до 17 р./сут, периодическое повышение температуры тела до 38° С в вечернее время. При колонофиброскопии от 15.03.2016 г. колоноскоп проведен в дистальный отдел восходящей части толстой кишки, заключение: эндоскопическая картина ЯК (тотальное поражение), тяжелая степень активности (рис. 2). При ЭГДС – хронический гастродуоденит с признаками выраженного обострения процесса, дуоденогастральный рефлюкс, недостаточность кардии, Нр+. Самостоятельно увеличил дозу месалазина до 4 г/сут, микроклизмы месалазина 2 г/сут на ночь со слабоположительным эффектом в виде урежения стула до 12 р./сут, примесь крови сохранялась.
![Рис. 1. Сцинтиграфия здорового добровольца. Будесонид MMX меченый [153Sm] в толстой кишке. Изображение получено через 7 ч после приема препарата (Brunner et al., 2006) Рис. 1. Сцинтиграфия здорового добровольца. Будесонид MMX меченый [153Sm] в толстой кишке. Изображение получено через 7 ч после приема препарата (Brunner et al., 2006)](https://www.rmj.ru/upload/medialibrary/fdc/fdce054cd022b9f2e7afc1c307ee002c.png)
18.03.2016 г. поступил на стационарное лечение в ГБУЗ МКНЦ ДЗМ. В общем анализе крови от 18.03.2016 г. отмечались лейкоцитоз (9,6 × 109) с палочкоядерным сдвигом (28%), повышение СОЭ до 26 мм/ч. В биохимическом анализе крови от 18.03.2016 г. отмечались повышение СРБ до 133,37 мг/л, латентный дефицит железа – 5,4 мкмоль/л.
При УЗИ органов брюшной полости 18.03.2016 г.: стенка левых отделов отечная, гипоэхогенная, утолщена до 7–8 мм, гаустрация сглажена, дифференциация слоев прослеживается четко не везде, в просвете – жидкость и изоэхогенное содержимое, в толще стенки – гиперэхогенные включения, что может соответствовать наличию язвенных дефектов; по ходу нисходящего отдела и сигмовидной кишки воспалительная инфильтрация параколической клетчатки с включением л/узлов размером до 11×7 мм; свободная жидкость в правой подвздошной области в небольшом количестве; заключение: эхопризнаки язвенного колита, левостороннее поражение, воспалительная инфильтрация параколической клетчатки по ходу левых отделов ободочной кишки с лимфаденопатией, небольшое количество свободной жидкости в правой подвздошной области (рис. 3). Кальпротектин кала от 19.03.2016 г. – 840 мкг/г.
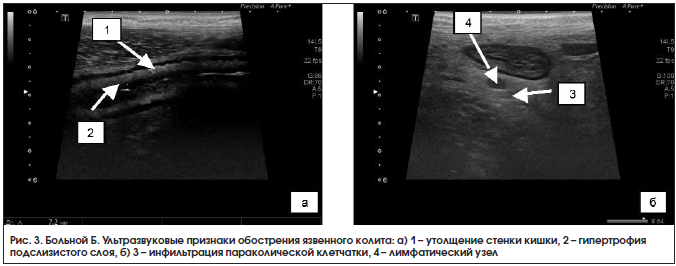
Установлен диагноз: язвенный колит, тотальное поражение, хроническое рецидивирующее течение, средней степени тяжести, умеренной активности. Латентный дефицит железа.
С учетом отсутствия у больного эффекта от терапии препаратами 5-АСК и категорического отказа от проведения терапии системными ГКС больному назначены Кортимент (топические ГКС) 9 мг/сут, месалазин 5 г/сут, микроклизмы с гидрокортизоном 125 мг 2 р./сут, метронидазол 500 мг 3 р./сут в/в, гидроксид железа 100 мг/сут № 3; цефтриаксон 2,0 г/сут в/в капельно.
На фоне терапии через 10 дней у больного отмечалось улучшение состояния в виде урежения стула до 2 р./сут, без примеси слизи и крови.
При контрольном УЗИ кишечника 28.03.2016 г.: по сравнению с предыдущим исследованием от 18.03.2016 г. отмечается положительная динамика. Тонкая кишка: петли не расширены, прослеживается ритмичная перистальтика, содержимое – средней эхогенности. Осмотрена ободочная кишка. В проекции слепой кишки, восходящего и поперечного отдела стенки не утолщены (2 мм), дифференциация слоев четкая. В проекции нисходящего отдела и сигмовидной кишки стенки толщиной 2,5–2,7 мм, слоистость стенки сохранена, более выражен подслизистый слой, в толще стенки сохраняются гиперэхогенные включения до 1,5 мм (вероятно, язвы). Клетчатка вокруг умеренно повышенной эхогенности с включением л/узлов размером до 8×3 мм. В правой подвздошной области межпетельно незначительное количество свободной жидкости. Заключение: эхопризнаки язвенного колита, левостороннее поражение, обострение. Мезентериальная лимфаденопатия (рис. 4). В общем анализе крови от 28.03.2016 г. сохраняется повышение СОЭ до 33 мм/ч. В биохимическом анализе крови от 28.03.2016 г. – нормализация уровня СРБ до 3,25 мг/л.
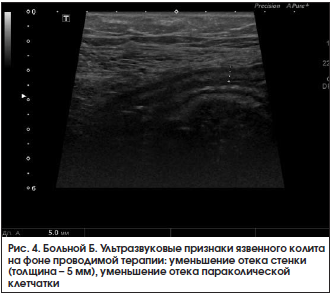
Заключение
Лекарственная формула будесонид ММХ доставляет лекарственное вещество в толстую кишку на всем ее протяжении [23], в то время как другие пероральные формы будесонида с контролируемым высвобождением работают только в дистальной части подвздошной кишки и в восходящей кишке – участках, которые наиболее часто поражаются воспалительным процессом при БК [24].
Будесонид ММХ является эффективным и хорошо переносится при применении с целью индукции ремиссии у пациентов с ЯК легкой и средней тяжести. Имеющиеся в настоящее время данные говорят о том, что этот препарат может быть эффективным и хорошо переноситься для поддержания длительной ремиссии (более 1 года) у пациентов с ЯК [17, 18]. Долгосрочная безопасность ММХ будесонида у пациентов с ЯК сравнима с таковой плацебо, эти данные представлены только в одном исследовании, которое длилось 12 мес. [19]. Однако в нескольких исследованиях изучали применение пероральных форм будесонида в качестве поддерживающей терапии у пациентов с БК, и это подтверждает долгосрочную (до 1 года) безопасность будесонида при поддержании ремиссии ВЗК [25–32]. Применение будесонида ММХ также может быть полезным в фармакоэкономическом плане в связи с возможным повышением приверженности терапии благодаря однократному приему препарата и снижению риска побочных явлений по сравнению с таковым при приеме традиционных пероральных кортикостероидов. Однако необходимо дальнейшее изучение этого препарата у пациентов с ВЗК.
Источник
- Симптомы
- Правильная диагностика
- Лечение
- Осложнения
- Профилактика
- Прогноз
 Неспецифический язвенный колит (НЯК) – хроническое воспаление толстого кишечника, сопровождающееся язвенными изменениями слизистой, прогрессирующими осложнениями (сужение, кровотечения, сепсис).
Неспецифический язвенный колит (НЯК) – хроническое воспаление толстого кишечника, сопровождающееся язвенными изменениями слизистой, прогрессирующими осложнениями (сужение, кровотечения, сепсис).
НЯК страдают чаще городские жители. Заболевание выявляется в основном в развитых индустриальных странах. Частота встречаемости 40-70 случаев на 100000 населения. Женщины болеют язвенным колитом в 1,5 чаще мужчин.
Существует несколько версий возникновения НЯК.
- Инфекционная природа. Предполагают, что язвенный колит – заболевание инфекционной природы. Изучаются вирусы, бактерии. Однако точного возбудителя НЯК выявить не удалось.
- Аутоиммунное заболевание. Существует мнение, что болезнь возникает из-за действия собственных антител. Организм воспринимает слизистую оболочку кишечника как чужеродную ткань.
- Наследственность. Считается, воспаление толстого кишечника имеет генетическую предрасположенность.
- Существует ряд факторов риска, которые являются спусковым механизмом для развития НЯК:
- несбалансированное питание, бедное пищевыми волокнами;
- стрессы;
- механические повреждения слизистой толстого кишечника;
- операции на толстом кишечнике;
- дисбиоз и хронические кишечные инфекции.
Симптомы и клиническая картина
Начало заболевания может быть острым. В последующем болезнь принимает хроническое течение. В зависимости от уровня поражения выделяют формы НЯК:
- проктит – поражение прямой кишки;
- проктосигмоидит – сочетанное поражение сигмовидной и прямой кишки;
- полное (тотальное) поражение.
Главный симптом неспецифического язвенного колита – частый жидкий стул с кровью и слизью.
 В период обострения болезни отмечается повышение температуры тела. Частота стула достигает 30 раз в сутки. Быстро наступает обезвоживание и анемия.
В период обострения болезни отмечается повышение температуры тела. Частота стула достигает 30 раз в сутки. Быстро наступает обезвоживание и анемия.
Нередко обострение менее выражено. Стул 1- 4 раза в сутки. Больной ощущает дискомфорт в животе и прямой кишке, снижается аппетит. Наблюдается потеря веса и общее недомогание.
Обильные кровотечения при язвенном колите наблюдаются редко, т. к. крупные сосуды не повреждаются. Однако длительное выделение крови со стулом приводит к железодефицитной анемии. У больных НЯК отмечается бледность, сухость кожи и слизистых, отмечается ломкость ногтей и волос, возможно извращение аппетита (желание есть несьедобные предметы и вещества).
Боль в животе для неспецифического язвенного колита не характерна. Появление абдоминальных болей говорит о развивающемся осложнении – перфорации стенки кишечника.
Диагностика заболевания
 Диагноз НЯК установить сложно. Для подтверждения заболевания проводят осмотр, лабораторную и инструментальную диагностику, проводят забор биопсийного материала.
Диагноз НЯК установить сложно. Для подтверждения заболевания проводят осмотр, лабораторную и инструментальную диагностику, проводят забор биопсийного материала.
При осмотре больного отмечается бледность и сухость кожных покровов, увеличенная частота пульса, повышение температуры. Живот вздут. При осмотре анального отверстия отмечается отечность и мокнутие, обнаруживаются анальные трещины.
Лабораторная диагностика является вспомогательной и позволяет заподозрить НЯК. Больному обязательно проводятся исследования крови и кала.
- Общий анализ крови. Характерно повышение СОЭ, анемия, повышение количества палочкоядерных лейкоцитов.
- Анализ кала проводят для выявления следов крови, слизи и оценки пищеварительной функции. Обнаружение в кале большого количества эритроцитов и слизи говорит в пользу НЯК.
- Биохимический анализ крови. Выявляются признаки обезвоживания – снижение магния, натрия, калия, хлора. Также снижается уровень холестерина и альбумина. Одновременно повышается уровень гамма-глобулинов в крови, что говорит об остроте воспаления.
Инструментальные методы исследования обязательны для постановки и уточнения диагноза. Больному с подозрением на неспецифический язвенный колит проводят ректороманоскопию, колонофиброскопию, ирригоскопию.
- Ректороманоскопия – эндоскопический метод исследования прямой кишки. Язвенный колит всегда начинается с прямой кишки, поэтому этого метода часто бывает достаточно. При исследовании обнаруживаются характерные изменения слизистой – отечность, гиперемия, эрозии и кровоизлияния.
- Фиброколоноскопия – эндоскопия толстого кишечника. Данное обследование можно проводить только при стихании обострения, т.к. при проведении процедуры высок риск повреждения слизистой и перфорации стенки кишки.Фиброколоноскопия позволяет установить протяженность патологического процесса. Также при данном исследовании проводится забор материала для биопсии.
- Ирригоскопия – рентгенологическое исследование толстого кишечника. При проведении этого обследования выявляются сужения, полипы, опухоли. По данному исследованию НЯК можно только заподозрить. Кроме того, для проведения ирригоскопии в качестве контрастного вещества применяется барий. Он противопоказан больным с активным колитом и при перфорации стенки кишечника.
- Обзорная рентгенография живота проводится для выявления перфорации кишечника.
Лечение
 Консервативное (терапевтическое) лечение зависит от степени тяжести и длительности течения болезни. Терапия направлена на скорейшее восстановление слизистой и возвращение пациента к нормальной жизни.
Консервативное (терапевтическое) лечение зависит от степени тяжести и длительности течения болезни. Терапия направлена на скорейшее восстановление слизистой и возвращение пациента к нормальной жизни.
Адекватный режим. Строго рекомендуется избегать физических и эмоциональных нагрузок.
Лечебное питание. Пища должна содержать большое количество белка. Еда должна быть протертой или мелкоизмельченной, отварной или приготовленной на пару. Полностью исключаются консервы, копчености, газообразующие продукты (горох, соя, бобы), сырые овощи и фрукты.
Парентеральное питание назначается в тяжелых случаях, когда пациент сильно истощен и не способен принимать пищу самостоятельно.
Медикаментозная терапия включает сульфасалазин, препараты 5-АСК (салофальк, месазалин), кортикостероиды (дексаметазон, преднизолон), цитостатики.
Сульфасалазин эффективен при легком и среднетяжелом НЯК. Терапевтическая доза 3 г. Препарат назначается на 4 недели, в последующем дозу постепенно снижают до 0,5-1,5 г в день. Эту дозировку больной получает длительное время для профилактики рецидивов.
Препараты 5-АСК также эффективны при легком и среднетяжелом колите. Дозировка 1,5-2,0 г в день. Преимущество 5-АСК в том, что она имеет меньше побочных эффектов, чем сульфазалазин.
Глюкокортикостероиды назначаются для лечения тяжелой формы неспецифического язвенного колита. Внутривенно вводят гидрокортизон в дозе 200мг/сут. При улучшении состояния, больного переводят на таблетки преднизолона. Доза 0,5-1 мг/сут.
Цитостатики используют только при крайне тяжелом течении колита. Эти препараты вызывают сильный иммунодефицит.
Дополнительно проводится симптоматическая терапия, она направлена на улучшение моторики кишечника, устранение анемии и обезвоживания, уменьшение кровопотери. В лечении НЯК используют:
- спазмолитики (но-шпа);
- кровоостанавливающие препараты (дицинон);
- препараты железа (мальтофер, сорбифер);
- противодиарейные средства (лоперамид, лопедиум).
Антибактериальная терапия проводится в случае присоединения вторичной инфекции.
Не забывайте, что одним препаратом невозможно «пролечить» такое заболевание. Лечение должно быть комплексным и проводиться под наблюдением врача.
Хирургическое лечение проводится при неэффективности консервативной терапии. Продолжающееся ректальное кровотечение с потерей крови более 100 мл/сутки является показанием для проведения колоэктомии.
Колоэктомия с резекцией прямой кишки – калечащая операция, в ходе которой полностью удаляется весь толстый кишечник, на переднюю брюшную стенку выводится колостома. Операция выполняется крайне редко у ограниченной группы пациентов.
Избежать операции можно только одним способом: не затягивать с болезнью, не заниматься самолечением, обращаться к врачу и полностью выполнять его рекоммендации. НЯК – тяжелое хроническое заболевание, приводящее к не менее тяжелым осложнениям. Лечение длительное и рисковать своим здоровьем не стоит.
Осложнения заболевания
Неспецифический язвенный колит может приводить к тяжелым осложнениям. При несвоевременном лечении развивается тяжелая анемия. В редких случаях может развиться угрожающее жизни кровотечение.
Перфорация стенки кишки сопровождается выходом содержимого кишечника в брюшную полость и раздражением брюшины. Основной симптом, указывающий на перфорацию – сильная боль в животе. Развивается перитонит и сепсис.
Длительно текущий воспалительный процесс приводит к изменению слизистой кишечника, сужению его просвета. На фоне пораженной слизистой начинают расти полипы и опухоли.
Дилатация (расширение) кишечника при длительном НЯК приводит к застою содержимого и всасыванию токсинов в кровь. У больного развивается стойкий интоксикационный синдром.
Внекишечные осложнения выражаются в поражении суставов, печени и желчных ходов.
Профилактика рецидивов
 Больные НЯК нуждаются в осмотре и коррекции медикаментозной терапии у гастроэнтеролога 1 раз в 4 месяца. С целью раннего выявления опухолей всем больным неспецифическим язвенным колитом ежегодно проводится колоноскопия.
Больные НЯК нуждаются в осмотре и коррекции медикаментозной терапии у гастроэнтеролога 1 раз в 4 месяца. С целью раннего выявления опухолей всем больным неспецифическим язвенным колитом ежегодно проводится колоноскопия.
Рекомендуется соблюдать режим дня. Придерживаться принципов лечебного питания. Больным следует продолжать прием лекарственных препаратов в поддерживающей дозе не менее полугода.
Пациенты с легкой формой заболевания переводятся на легкий труд. Больные более тяжелыми формами НЯК признаются нетрудоспособными. Тем не менее современная медицина может обеспечить пациенту с НЯК хорошее качество жизни.
Прогноз
Прогноз неспецифического язвенного колита зависит от тяжести и длительности течения, наличия осложнений. Считается, что худший прогноз имеет НЯК, проявившийся в раннем детстве и в возрасте старше 60 лет.
Источник


