Ванкомицин при псевдомембранозном колите
Резюме. Псевдомембранозный колит (ПМК) — редкое, но опасное заболевание, вызванное микробом Clostridium difficile (C. difficile).
C. difficile in vitro проявляют различную чувствительность к антибиотикам, однако наиболее стабильная чувствительность наблюдается к ванкомицину и метронидазолу. Несмотря на то что ванкомицин обычно назначают в дозе по 500 мг, проведенные исследования показывают, что дозы 125 мг 4 раза в сутки бывает вполне достаточно для купирования воспаления. Прием ванкомицина предпочтителен в тяжелых случаях ПМК. Курс лечения антибиотиками составляет 10 дней. Если невозможен пероральный прием препаратов, их вводят через назогастральный зонд. В редких случаях, при тяжелом течении ПМК, возможно комбинированное применение ванкомицина (per rectum) и метронидазола (внутривенно), но следует помнить, что внутривенное введение препаратов менее эффективно.
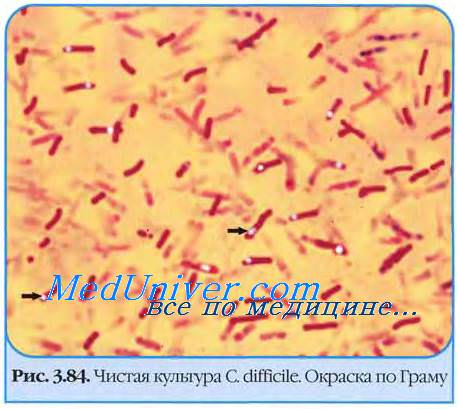
 Псевдомембранозный колит (ПМК) — редкое, но опасное заболевание, вызванное микробом Clostridium difficile (C. difficile). C. difficile — достаточно крупные (от 0,5–1,9 до 3,0–16,9 мкм) подвижные грамположительные бактерии, относящиеся к группе облигатных анаэробов (род Clostridium), образующие в неблагоприятных условиях овальные субтерминальные споры, которые устойчивы к нагреванию и способны к длительному (в течение нескольких лет) выживанию в аэробных условиях. Температурный оптимум роста вегетативных форм — 30–37 °С.
Псевдомембранозный колит (ПМК) — редкое, но опасное заболевание, вызванное микробом Clostridium difficile (C. difficile). C. difficile — достаточно крупные (от 0,5–1,9 до 3,0–16,9 мкм) подвижные грамположительные бактерии, относящиеся к группе облигатных анаэробов (род Clostridium), образующие в неблагоприятных условиях овальные субтерминальные споры, которые устойчивы к нагреванию и способны к длительному (в течение нескольких лет) выживанию в аэробных условиях. Температурный оптимум роста вегетативных форм — 30–37 °С.
C. difficile широко распространены в природе, являясь постоянными обитателями кишечника многих видов животных (домашних и диких), а в некоторых случаях выявляются и в испражнениях здоровых людей различного возраста, включая новорожденных. Как показывают наблюдения, 3–6% здоровых людей являются носителями C. difficile. В стационарах частота выявления бактерионосителей C. difficile может быть выше. Здоровые дети первого года жизни, в том числе новорожденные, являются носителями C. difficile гораздо чаще — в 30–90%.
Несмотря на то что C. difficile не относятся к патогенным бактериям, тем не менее в определенных условиях они способны вызывать такие заболевания, как антибиотикоопосредованная диарея и ПМК.
Условия, необходимые для развития инфекции C. difficile, в том числе и ПМК:
- наличие источника инфицирования;
- пероральный прием антибиотиков или других групп препаратов, способных вызвать нарушение микробиоценоза кишечника;
- колонизация слизистой оболочки толстой кишки C. difficile и выработка экзотоксинов;
- индивидуальные факторы риска: возраст, предшествующие заболевания и госпитализации, длительность заболевания.
Хотя риск инфицирования при прямом контакте с бактериовыделителем или больным, как правило, невысок, однако длительный контакт может привести к развитию клинически манифестных форм инфекций, обусловленных C. difficile.
Имеются убедительные данные, свидетельствующие о том, что C. difficile не способны к длительному существованию в неизмененной нормальной микроэкосистеме кишечника. Критическим фактором для развития инфекции C. difficile, в том числе и ПМК, является снижение колонизационной резистентности кишечника, в частности толстой кишки, как следствие нарушения микробиоценоза.
Антибиотикотерапия предшествует развитию ПМК в 60–85% случаях. ПМК развивается, как правило, либо непосредственно на фоне проводимой антибиотикотерапии, либо через 7–10 дней (в редких случаях позже) после прекращения антибиотикотерапии. Чаще всего развитие инфекции C. difficile отмечается на фоне приема цефалоспоринов III поколения, клиндамицина, ампициллина, амоксициллина с клавулановой кислотой, фторхинолонов. Макролиды и рифампицин достаточно редко выступают в роли кофакторов в развитии инфекции C. difficile. Следует помнить, что ни доза, ни кратность, ни даже способ введения препарата не влияют на возможность развития инфекции C. difficile. Были случаи, когда даже однократное введение антибиотика приводило к развитию антибиотикоопосредованной диареи и ПМК. Согласно наблюдениям, ПМК развивается у амбулаторных больных при применении пероральных антибиотиков с частотой 1–3 случая на 100 тыс. больных, а среди госпитализированных пациентов частота развития ПМК составляет 1 на 100 (в зависимости от профиля стационара).
Кроме того, описаны случаи развития инфекции C. difficile, в том числе и ПМК, при применении химиотерапии, антинеопластических препаратов, иммуносупрессивной терапии, препаратов золота, нестероидных противовоспалительных препаратов, антидиарейных средств, нейролептиков. Нарушение микроэкологии кишечника, сопровождающееся колонизацией C. difficile, отмечается при обширных операциях на брюшной полости, длительном использовании назогастральных зондов и клизм, у пациентов реанимационных отделений и отделений интенсивной терапии, при почечной недостаточности и некоторых других состояниях.
Практика показывает, что наиболее часто инфекция C. difficile выявляется в хирургических стационарах, особенно у больных, перенесших операцию на кишечнике. Данное обстоятельство может иметь только одно объяснение: помимо того что обширные хирургические операции сами по себе могут способствовать развитию инфекции C. difficile, такие больные более чем в 90% получают антибиотики широкого спектра действия как с целью лечения, так и профилактики. И все же примерно у 10–11% хирургических больных инфекция C. difficile развивается без предварительного применения антибиотиков.
Ведущими факторами патогенности C. difficile являются токсические субстанции, вырабатываемые C. difficile: токсин А (ТА) и токсин В (ТВ), которые in vivo проявляют синергизм действия. ТА — это мощный энтеротоксин с цитотоксической активностью, вызывающий нарушение барьерной функции слизистой оболочки кишечника за счет повреждения эпителиоцитов и активацию секреции жидкости в просвет кишечника. ТВ — в 1000 раз более мощный цитотоксин, чем ТА, однако его цитотоксический эффект обусловлен нарушением полимеризации внутриклеточных филаментов актина. Выявляемые в толстой кишке морфологические изменения слизистой оболочки обусловлены действием только токсинов, поскольку сами C. difficile не обладают инвазивными свойствами и, как правило, в подслизистый слой не проникают. Протяженность и глубина морфологических изменений, выявляемых в толстой кишке, обусловливают тяжесть течения инфекционного процесса.
Средний возраст заболевших составляет 58–60 лет, хотя развитие инфекции C. difficile принципиально не зависит от возраста больных. Исключение составляют новорожденные и дети в возрасте до 1 года, у которых развитие инфекции C. difficile является нетипичным (в данной возрастной группе в кишечном эпителии отсутствуют рецепторы для токсинов C. difficile).
Спектр клинических проявлений инфекции C. difficile варьирует в широких пределах: от бессимптомного носительства и самокупирующейся диареи — до тяжелого колита. ПМК представляет собой крайнюю форму проявления инфекции C. difficile с возможным рецидивирующим течением, часто неблагоприятным прогнозом и требует особо сложного лечения.
Факторы риска развития колита, обусловленного C. difficile:
- Возраст старше 65 лет
- Почечная недостаточность
- Хроническая обструктивная болезнь легких
- Злокачественные новобразования
- Прием блокаторов Н2-гистаминовых рецепторов
- Поступление больных из других стационаров
- Пребывание больного в отделении интенсивной терапии
Типичными для ПМК являются жидкий стул, боль в животе и лихорадка. В клинической картине ПМК доминирует диарейный синдром (в дебюте заболевания выявляют в 100% случаев), который в отдельных случаях бывает единственным проявлением заболевания. Частота дефекаций в сутки достигает ≥5 раз, доходя иногда до 20–30. Стул, как правило, небольшого объема, водянистый, часто содержит примесь слизи, тогда как примесь крови не характерна. Диарея носит упорный характер и может сохраняться до 8–10 нед. В отдельных случаях расстройство стула может носить перемежающий характер, когда диарея сменяется оформленным стулом, сохраняющимся в течение 1–2 дней. Рвота отмечается достаточно редко и в более поздние сроки заболевания, свидетельствуя о тяжести его течения. Учитывая длительный и упорный характер диареи, у больных с ПМК часто выявляются тяжелые электролитные расстройства (гипокалиемия), гиповолемия, снижение уровня альбуминов в плазме крови, развитие отеков вплоть до анасарки, гипотензия.
Фактически одновременно с диарейным синдромом у больных отмечается боль в животе разной интенсивности, преимущественно спастического характера, выраженность которой усиливается при пальпации живота. Чаще всего боль не имеет четкой локализации и определяется по ходу кишечника.
В единичных случаях манифестация заболевания может начинаться с лихорадки. В большинстве случаев температура тела у больных с ПМК держится на фебрильных цифрах, однако в последние годы участились случаи заболевания, при которых регистрируется гектическая лихорадка, превышающая 40 °С.
Характерным для ПМК является достаточно выраженный лейкоцитоз периферической крови, достигающий 15·109/л, а в ряде случаев выявляются даже лейкемоидные реакции, при которых количество лейкоцитов может достигать 40·109/л. Имеются отдельные наблюдения, когда ПМК у больных развивается на фоне лейкопении. Как правило, лейкопения регистрируется у больных, получавших химиотерапию по поводу злокачественных опухолей. Течение ПМК у этих пациентов исключительно тяжелое и часто носит фульминантный характер с развитием бактериемии. Именно фульминантное течение ПМК представляет наибольшую трудность относительно диагностики в силу необычности выявляемой клинической симптоматики, поскольку в этом случае наблюдается комбинированное поражение толстой и тонкой кишки.
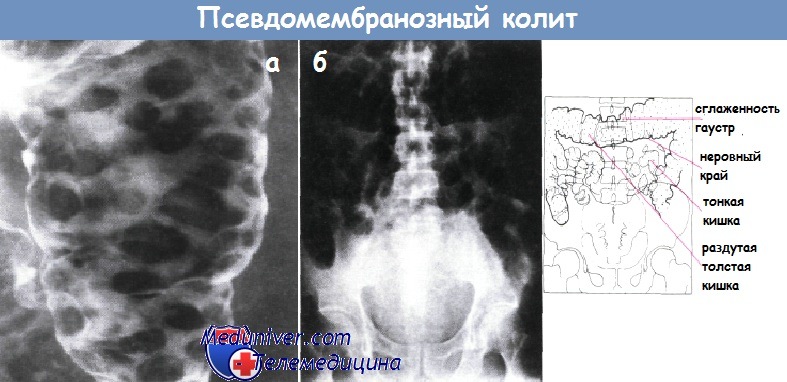
Для фульминантного течения ПМКхарактерно быстрое прогрессирование процесса. Диарейный синдром, являющийся ключевым для антибиотикоопосредованной диареи, при фульминантном течении ПМК может отсутствовать. Почти у половины больных регистрируют запор и признаки кишечной непроходимости. У этих пациентов выявляют признаки «острого живота», лихорадка бывает выше 38,4 °С. При компьютерной томографии брюшной полости выявляется асцит и значительное утолщение стенки толстой кишки. Несмотря на отчетливые клинические признаки «острого живота», свободный воздух в брюшной полости не определяется. Летальность при фульминантном течении ПМК достигает 58%.
ПМК может осложняться развитием токсического мегаколона, перфорацией толстой кишки с развитием перитонита, инфекционно-токсическим шоком.
Рецидивирующее течение ПМК отмечается в 20% у больных с первично установленным диагнозом после проведения стандартной антибиотикотерапии. Для больных, у которых выявлен хотя бы один рецидив, риск рецидивирующего течения ПМК возрастает до 45–68%. Механизм формирования рецидивирующего течения ПМК до сих пор до конца не выяснен. Полагают, что основной причиной является неполная санация кишечника от спор C. difficile, хотя не исключается возможность реинфицирования.
Факторы риска развития рецидивирующего течения ПМК:
- Наличие в анамнезе предшествующих эпизодов диареи, обусловленной C. difficile
- Заболевания, обусловленные 1 или 2 типом штамма C. difficile
- Длительные курсы антибиотикотерапии в анамнезе при лечении других инфекционных заболеваний
- Женский пол
- Начало заболевания весной
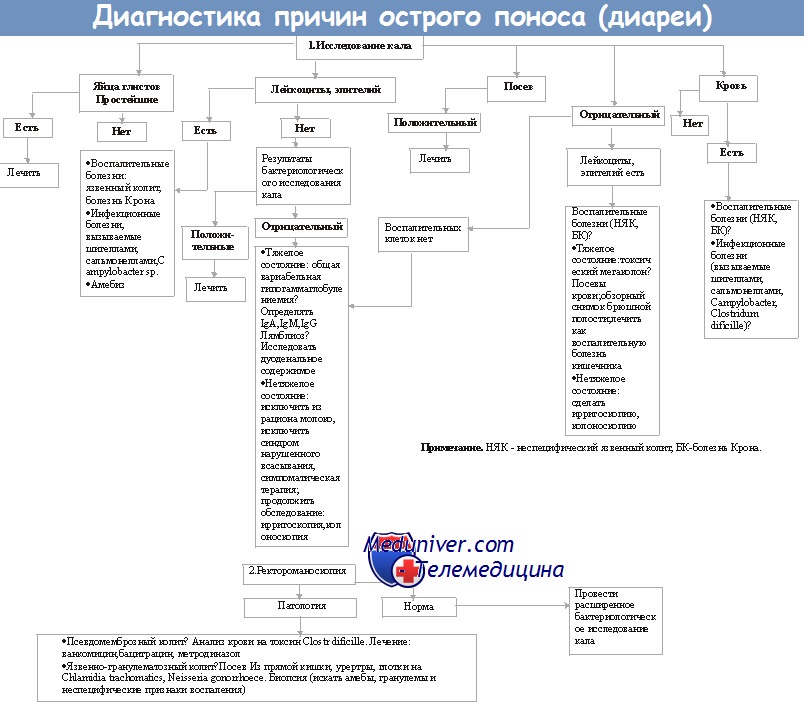
Диагностика инфекции C. difficile является сложной проблемой. Выделение возбудителя хоть и представляется важным, но имеет второстепенное значение в связи с медленным ростом бактерий. Важнейшим методом верификации диагноза ПМК является выявление токсинов C. difficile в стуле. Токсигенные штаммы C. difficile, вызывающие развитие ПМК, вырабатывают, как правило, оба токсина, однако золотым стандартом в диагностике ПМК может служить определение ТВ при тестировании культуры клеток, которое представляет собой наиболее чувствительный метод. В последние годы разрабатываются методы полимеразной цепной реакции как альтернатива цитотоксическому тесту.
Не утратили своего диагностического значения эндоскопические методы. Патологические изменения локализуются преимущественно в дистальном отделе толстой кишки, и для их выявления достаточно провести сигмоидоскопию, однако у ⅓ больных патологические изменения локализуются только в проксимальном участке толстой кишки; в этом случае требуется проведение колоноскопии. Тонкая кишка также может вовлекаться в патологический процесс, однако данный факт выявляется только на аутопсии. При сигмоидоскопии и колоноскопии отмечают диффузную гиперемию и отечность слизистой оболочки кишечника с утолщением стенки кишки, хотя в стенке кишки выявляется незначительная воспалительная реакция, а в подслизистом слое — скопление лимфоцитов. На поверхности выявляют характерные фибринозные бляшки желтовато-белого цвета в диаметре от 2 мм до ≥2 см, покрывающие язвы слизистой оболочки кишечника. Эти бляшки могут сливаться, образуя псевдомембранозные поля. Псевдомембраны выявляются между прямой кишкой и левым изгибом ободочной кишки, но может поражаться и поперечная ободочная кишка.
При установлении диагноза ПМК лечение начинают незамедлительно. Прежде всего, если заболевание развилось на фоне антибиотикотерапии, необходима ее отмена. Характер и объем проводимых терапевтических мероприятий у пациентов с инфекцией C. difficile определяются клиническим вариантом заболевания. Асимптоматическое носительство, как правило, не требует специальных методов лечения.
Проводимая больным ПМК терапия преследует две основные цели: во-первых, необходимо купировать воспалительный процесс в кишечнике и, во-вторых, санировать кишечник от спор C. difficile.
Несмотря на то что антибиотики чаще всего служат причиной развития инфекции C. difficile, именно антибактериальная терапия является неотъемлемой частью стандартной базисной терапии ПМК, проведение которой ограничивает колонизацию кишечника C. difficile и купирует воспалительные изменения в кишечнике. Базисная антибактериальная терапия способствует достаточно быстрому купированию клинических проявлений заболевания: нормализация температуры тела наступает, как правило, уже в течение 24–48 ч, а частота и характер стула восстанавливаются на 1–13-й день (в среднем — 4,5 дня). У больных с фульминантным течением ПМК базисная терапия часто оказывается малоэффективной, поэтому в таких случаях проводят хирургическое лечение.
Обязательным условием проведения этиотропной терапии у больных с ПМК является энтеральное введение антибиотиков, поскольку при парентеральном их введении в кишечнике не создается достаточной концентрации и санация организма не наступает.
C. difficile in vitro проявляют различную чувствительность к антибиотикам, однако наиболее стабильная чувствительность наблюдается к ванкомицину и метронидазолу. В качестве базисной антибактериальной терапии можно применять и бацитрацин, однако в силу вариабельности и нестабильности фармакологического эффекта относительно C. difficile предпочтение отдают метронидазолу и ванкомицину. Несмотря на то что ванкомицин обычно назначают в дозе по 500 мг, проведенные исследования показывают, что дозы 125 мг 4 раза в сутки бывает вполне достаточно для купирования воспаления.Прием ванкомицина предпочтителен в тяжелых случаях ПМК. Курс лечения антибиотиками составляет 10 дней. Если невозможен пероральный прием препаратов, их вводят через назогастральный зонд. В редких случаях, при тяжелом течении ПМК, возможно комбинированное применение ванкомицина (per rectum) и метронидазола (внутривенно), но следует помнить, что внутривенное введение препаратов менее эффективно.
По материалам публикации Малова В.А. и соавт.
(Лечащий врач, 1999, 2–3), предоставленной компанией «ТЕВА УКРАИНА».
Источник
Клостридиальный псевдомембранозный колит (С. difficile-ассоциированный колит)Псевдомембранозный или С. difficile-ассоциированный колит представлен широким спектром клинических проявлений от умеренной диареи до фульминантной формы с возможным фатальным исходом. В «доантибиотическую» эру псевдомембранозный колит вызывался различными возбудителями (например, Staphylococcus); в настоящее время наиболее типичной причиной является избыточное размножение симбионтного анаэроба С. difficile на фоне антибиотикотерапии. Патофизиология: гибель нормальных бактерий толстой кишки, вызвванная антибиотиками (от нескольких дней до 10 недель после приема антибиотиков), приводит к колонизации токсинпродуцирующим С. difficile (орально-фекальный путь заражения). Высвобождение токсинов А и В приводит к гибели слизистой и воспалению. В основе различных степеней проявления заболевания лежат: 1) иммунные факторы хозяина и 2) вирулентные факторы микроорганизмов. Антибиотики, связанные с клостридиальным колитом: любые антибиотики (за некоторым исключением, например, ванкомицин); частота возникновения колита в значительной степени является отражением повсеместного использования соответствующих лекарственных препаратов: пенициллинов, цефалоспоринов, фторхинолонов, клиндамицина и даже метронидазола (несмотря на то, что последний применяется для лечения при С. difficile). Лечение: от консервативного (легкие и среднетяжелые формы) до колэктомии (тяжелые и жизнеугрожающие формы), которая может спасти больному жизнь.
а) Эпидемиология: б) Симптомы псевдомембранозного колита: — Заболевание с различной степенью тяжести и динамикой развития (бессимптомное, самокупирующееся/ограниченное кишечником, прогрессирующее/системное, хроническое «тлеющее»/системное, фульминантное, с развитием полиорганной недостаточности): — Осложнения: дилатация толстой кишки (вначале картина как при синдроме Огилви) => токсический мегаколон, перфорация, сепсис, олигурия, полиорганная недостаточность, смерть. — Редкие формы:
в) Дифференциальный диагноз клостридиального колита: г) Патоморфология псевдомембраного колита Микробиология Clostridium difficile: • С. difficile повсеместно распространенный грамположительный анаэроб, образующий устойчивые к нагреванию споры, способные сохраняться в окружающей среде месяцы и годы => отличие патогенных штаммов от непатогенных состоит в способности продуцировать токсины, вызывающие диарею и колит. • Инфицирование происходит при проглатывании спор, которые могут выжить в кислой среде желудка и развиться в вегетативные формы в толстой кишке. • Наличие С. difficile обычно для окружающей среды больниц/учреждений длительного ухода: • Токсины: Макроскопическое/микроскопическое исследование:
д) Обследование при псевдомембранозном колите Необходимый минимальный стандарт: 1. Диарея. Анализ кала на токсины С. difficile А и В (посев С. difficile не показан!). 2. Диарея и абдоминальные/системные или неопределенные симптомы: Дополнительные исследования (необязательные):
е) Классификация псевдомембранозного колита: ж) Лечение без операции псевдомембраного колита 1. Амбулаторно или в стационаре при легких симптомах: 2. Стационар при выраженных сопутствующих заболеваниях/ПИТ: 3. Альтернативы:
и) Операция при псевдомембранозном колите Показания: Хирургический подход. Колэктомия с концевой илеостомой у всех без исключения больных. к) Результаты лечения клостридиального колита: л) Наблюдение и дальнейшее лечение: — Также рекомендуем «Инфекционный энтероколит — причины, признаки, лечение» Оглавление темы «Болезни толстой кишки»:
|
Источник