Гиперурикемия камни в почках
Одна из наиболее распространенных обменных патологий, представляющая собой увеличение в крови содержания мочевой кислоты, носит название гиперурикемии. Увеличение концентрации мочевой кислоты в крови (гиперурикемия), в зависимости от степени ее повышения, может протекать латентно и выявляться случайно при исследовании биохимического состава крови.
В других случаях гиперурикемия выявляется при появлении жалоб со стороны почек, суставов и других органов. Гиперурикемия влечёт за собой целый ряд процессов, запускающих каскад биохимических, а затем патофизиологических изменений, итогом которых является появление болезней, таких как подагра, уролитиаз (образование мочевых уратных камней в почках), нефропатия и другие состояния.
Мочевая кислота — вещество, появляющееся на заключительном, конечном этапе нормальных метаболических процессов, в которых принимают участие пурины, из которых она образуется. Путь выведения пуринов из организма — превращение их метаболитов в мочевую кислоту в паренхиме печени. Мочевая кислота фильтруется через почки, превращается в ураты (соли мочевой кислоты), которые затем вместе с мочой выводятся из организма.
Ураты — химические соединения, относящиеся к солям, предшественником которых является мочевая кислота. Ураты обладают способностью, при нормальной их концентрации, находиться в растворе, при этом их растворимость в моче может характеризоваться как средняя. При превышении концентрации солей мочевой кислоты особенность метаболизма уратов определяет возможность их выпадения в осадок из раствора (образование уратных микро- и макролитов).

Содержание мочевой кислоты у человека (в норме) ограничено значениями, не превышающими 0,42 ммоль/л у мужской половины населения, у женщин нормальное содержание мочевой кислоты меньше, порядка 0,36 ммоль/л. Ее концентрация в моче строго регламентирована, при превышении нормальных значений ураты могут инициировать патологический процесс преципитации и образования сначала микро- (песок), а затем и макролитов (камней) в почках.
Гиперурикемия в любых её проявлениях (как минимальном, так и при значительном её повышении) ведёт к патологии: откладываясь в тканях и органах, мочевая кислота приводит в последующем к появлению типичных симптомов.
Для понимания системности процессов, происходящих при гиперурикемии, рассмотрим наиболее частые причины, приводящие к избыточному содержанию в плазме крови мочевой кислоты.
Причины гиперурикемии (повышения содержания мочевой кислоты в крови):
- Одной из главных причин гиперурикемии считают индивидуальную особенность метаболизма пуринов данного индивидуума (обмена, выведения, синтеза мочевой кислоты и её солей), обусловленных генетическими особенностями организма.
У некоторых людей при прочих равных условиях и отсутствии избытка поступления пуринов с пищей может выявляться гиперурикемия. Причина этого явления кроется в особенностях метаболизма уратов у конкретного больного. Часто нарушение пуринового обмена обусловлено генной мутацией фермента, ответственного за выведение или дальнейшее превращение пуринов, либо нарушением механизма выведения солей уратов.
- Значительную роль в формировании гиперурикемии играет неправильное, избыточное питание, в котором превалируют белковые продукты, содержащие много пуринов, пища, богатая предельными тугоплавкими жирными кислотами (животный жир, субпродукты, желток).
Усиливается пагубное влияние избыточного потребления пуринов одновременным приёмом алкоголя. При этом риск гиперурикемии увеличивается, особенно если алиментарные погрешности сочетаются с наследственной предрасположенностью.
- Некоторые лекарственные средства, применяемые для лечения различных заболеваний сердца, повышенного давления, эндокринных патологий, могут давать побочный эффект в виде гиперурикемии. Например, хорошо известно гиперурикемическое действие тиазидных диуретиков, б-блокаторов.
И наоборот, существуют препараты, значимо снижающие повышенный уровень уратов (мочевой кислоты). К ним относятся урикозурические средства (выводящие мочевую кислоту) и препараты, уменьшающие её образование.
- Наконец, некоторые заболевания и патологические процессы могут вызвать гиперурикемию.
Важным является не только клинически значимая гиперурикемия, которая проявляется подагрой, нефроуролитиазом или уратной нефропатией, но и бессимптомная гиперурикемия.
Гиперурикемия входит в состав так называемого метаболического синдрома, включающего в себя повышение давления, ту или иную степень ожирения, повышение в крови атерогенных липопротеидов, появление гликемии (у одного человека может присутствовать несколько перечисленных факторов одновременно). Метаболический синдром — комплекс состояний, увеличивающих риск фатальных событий (смерти) в несколько раз. В последние годы частота выявления метаболического синдрома неуклонно растёт, гиперурикиемия при этом вносит значительный вклад в риски при метаболическом синдроме.
В среднем гиперурикемия может быть выявлена более чем у 6 % населения, но клинически значимые состояния и заболевания при документально повышенном уровне мочевой кислоты развиваются не во всех случаях.
Возникновение гиперурикемии может быть связано как с повышенным синтезом продуктов метаболизма пуринового обмена, так и с пониженной фильтрацией и экскрецией мочевой кислоты через нефроны почки. Увеличивается содержание пуринов при ряде онкологических заболеваний, псориазе, использовании цитостатических препаратов.
Симптомы гиперурикемии
Гиперурикемия чаще всего проявляется поражением суставов, что носит название «подагра», и нарушением функции почек (нефропатия, образование почечных камней).
Почечные проявления гиперурикемии
Повышенное выделение уратов с мочой оказывает повреждающее действие как на почечную интерстициальную ткань (уратная нефропатия), так и на чашечно-лоханочную систему мочевыводящей системы. Уратная нефропатия захватывает функциональную ткань — почечные нефроны (клубочки) и интерстиций, в результате чего выделительная и другие функции почек прогрессивно снижаются, появляются признаки и симптомы почечной недостаточности (чаще в виде хронической формы).
При сочетании уратной нефропатии и гиперурикемии с другими обменными патологиями — сахарным диабетом, атеросклерозом, патологиями почек — почечная недостаточность приобретает более злокачественное течение.
Нефроуролитиаз — самое частое проявление гиперурикемии. Чаще при образовании камней в почках гиперурикемия достигает значительной степени выраженности. Нефролитиаз — одно из частых заболеваний, вызванных наследственными дефектами метаболизма уратов в сочетании с диетическими погрешностями, использованием жёсткой питьевой и минеральной воды в течение длительного времени.
Почечные конкременты (камни) могут иметь разный состав. При гиперурикемии конкременты носят характер уратных образований. Начало формирования камней бессимптомное, ничем себя не проявляет. Образование микролитов, так называемого «песка», может инициироваться воспалением в чашках и лоханках, что имеет место при остром (чаще хроническом) пиелонефрите.
Уратные камни в почечных лоханках могут быть единичными и множественными, с одно- и двусторонней локализацией. Иногда уратный камень занимает всю полость лоханки. В таком случае конкремент носит название коралловидного.
Поражение почек при уратном нефролитиазе может усугубляться возможностью поддержания в почках хронического воспалительного процесса вследствие длительного нарушения оттока и стаза мочи, характеризующегося периодами ухудшения состояния (обострение) и ремиссий.
Острое затруднение оттока мочи из почки может возникнуть при миграции (движении) подвижных, мелких камней в мочеточник. Это состояние носит название «почечная колика», при которой больному требуется неотложная медицинская помощь. Нередко уратный нефролитиаз вследствие гиперурикемии впервые проявляется именно почечной коликой, так как до этого даже относительно крупные камни могут долго не давать о себе знать.
Почечная колика может быть спровоцирована такими факторами, как сотрясение тела (длительная тряская езда), прыжки, обильный приём жидкости, алкоголя, подъём тяжестей. У больного при почечной колике любого генеза, в том числе при камнях вследствие гиперурекимии, возникают острые, выраженные, нестерпимые боли в поясничной области. Часто при колике интенсивные боли отдают в пах, сопровождаются частым мочеиспусканием.
На высоте боли у больного с коликой возникает тошнота, часто рвота, повышается системное АД (давление). Цвет мочи может меняться, появляются примеси крови (необязательный симптом). Интенсивность болей в пояснице при колике такова, что больной мечется от боли, ищет помощи, не может найти положение, которое бы облегчило его страдания. При полной закупорке мочеточника конкрементом может возникнуть острое осложнение — гидронефроз.
Гиперурикемия и поражение суставов (подагра)
Поражение суставов при гиперурикемии носит название «подагра». Типичным именно для подагры является поражение в начале заболевания первого пальца стопы (плюснефалангового суставного сочленения). Подагрический артрит начинается остро, без предвестников, часто в ночное время с острой боли в указанном суставе. При этом сустав при подагре быстро краснеет, отекает, больной жалуется на распирающие, «стреляющие» боли, невозможность наступать на поражённую конечность, нарушается сон, трудоспособность невозможна.
После стихания островоспалительных явлений первой атаки (в результате лечения и снижения степени гиперурикемии) у больного наступает улучшение. Но в последующем при нарушении диеты (белковая, жирная пища, алкоголь) может наступить обострение суставного синдрома при подагре. Со временем, если гиперурикемия не компенсирована или прогрессирует, в процесс вовлекаются другие крупные суставы (коленные, голеностопы, локтевые). В них наблюдаются подобные воспалительные изменения вследствие хронической гиперурикемии и отложения в тканях суставов мочевой кислоты.
Также типичным для подагры считается формирование отложений в тканях уратов — появление так называемых тофусов. Тофусы при гиперурикемии могут образовываться в любом месте, часто вблизи суставов, на ушных раковинах. Чрезмерная гиперурикемия может приводить к тому, что тофусы самопроизвольно вскрываются с выделением масс, состоящих из кристаллов уратов.
Хроническая гиперурикемия также может способствовать отложению уратов в других органах и тканях, коже.
Таким образом, гиперурикемия — серьёзное состояние, требующее грамотного подхода, обязательной диагностики, коррекции и лечения. Гиперурикемия всегда приводит к поражению тканей и формированию хронических метаболических расстройств — подагры, нефроуролитиаза, уратной нефропатии — и к поражению суставных тканей. Важным является то, что гиперурикемия даже на доклиническом этапе оказывает неблагоприятное воздействие на организм.
При подозрении на гиперурикемию, при наличии метаболического синдрома и других состояниях, при которых нарушается обмен пуринов, обязательно исследование плазмы крови на содержание мочевой кислоты, проведение других функциональных тестов.
Источник
Самым частым нарушением обмена пуринов является повышенное образование мочевой кислоты с развитием гиперурикемии. Особенностью является то, что растворимость солей мочевой кислоты (уратов) в плазме крови невелика и при превышении порога растворимости в плазме (около 0,7 ммоль/л) они кристаллизуются в периферических зонах с пониженной температурой.
В зависимости от длительности и тяжести гиперурикемия проявляется:
- Появление тофусов (греч. tophus – пористый камень, туф) – отложение уратных кристаллов в коже и подкожных слоях, в мелких суставах ног и рук, в сухожилиях, хрящах, костях и мышцах.
- Нефропатии в результате кристаллизации мочевой кислоты с поражением почечных канальцев и мочекаменная болезнь.
- Подагра – поражение мелких суставов.
Для диагностики нарушений используют определение концентрации мочевой кислоты в крови и моче.
Нарушения обмена пуринов
Подагра
Когда гиперурикемия принимает хронический характер, говорят о развитии подагры (греч. poclos – нога, agra – захват, дословно – «нога в капкане»).
В крови мочевая кислота находится в форме ее солей – уратов натрия. Из-за низкой растворимости ураты способны оседать в зонах с пониженной температурой, например, в мелких суставах стоп и пальцев ног. Накапливающиеся в межклеточном веществе ураты некоторое время фагоцитируются, но фагоциты не способны разрушить пуриновое кольцо. В результате это приводит к гибели самих фагоцитов, к выходу лизосомальных ферментов, активации свободнорадикального окисления и развитию острой воспалительной реакции – развивается подагрический артрит. В 50-75% случаев первым признаком заболевания является мучительная ночная боль в больших пальцах ног.
Длительное время подагру считали «болезнью гурманов», однако затем внимание исследователей переместилось к наследственному изменению активности ферментов метаболизма пуринов:
- увеличение активности ФРДФ-синтетазы – приводит к избыточному синтезу пуринов,
- уменьшение активности гипоксантин-гуанин-фосфорибозил-трансферазы – из-за этого ФРДФ не используется для реутилизации пуриновых оснований, а участвует в первой реакции их синтеза. В результате возрастает количество разрушающихся пуринов и одновременно повышается их образование.
Оба ферментативных нарушения рецессивны и сцеплены с X-хромосомой. Подагрой страдает 0,3-1,7% взрослого населения земного шара, соотношение заболевших мужчин и женщин составляет 20 : 1.
Основы лечения
Диета – снижение поступления предшественников мочевой кислоты с пищей и уменьшение ее образования в организме. Для этого из рациона исключаются продукты, содержащих много пуриновых оснований – пиво, кофе, чай, шоколад, мясные продукты, печень, красное вино. Предпочтение отдается вегетарианской диете с количеством чистой воды не менее 2 л в сутки.
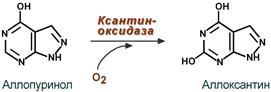
Реакция превращения аллопуринола
К лекарственным средствам лечения подагры относят аллопуринол, по структуре схожий с гипоксантином. Ксантиноксидаза окисляет аллопуринол в аллоксантин, и последний остается прочно связанным с активным центром фермента и ингибирует его. Фермент осуществляет, образно говоря, самоубийственный катализ. Как следствие, ксантин не превращается в мочевую кислоту, и поскольку гипоксантин и ксантин лучше растворимы в воде, то они более легко выводятся из организма с мочой.
Мочекаменная болезнь
Мочекаменная болезнь заключается в образовании солевых кристаллов (камней) разной природы в мочевыводящих путях. Непосредственно образование мочекислых камней составляет около 15% от всех случаев этой болезни. Мочекислые камни в мочевыводящих путях откладываются примерно у половины больных подагрой.
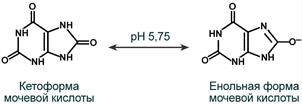
Две переходные формы мочевой кислоты при pH 5,75
Наиболее часто такие камни представлены в дистальных канальцах и собирательных трубочках. Причиной отложения кристаллов мочевой кислоты является гиперурикемия и повышенное выведение уратов натрия с мочой. Главным провоцирующим фактором кристаллизации является увеличение кислотности мочи. При понижении рН мочи ниже 5,75 ураты (енольная форма) переходят в менее растворимую кетоформу и кристаллизуются в почечных канальцах.
Закисление мочи (в норме 5,5-6,5) возникает по различным причинам. Это может быть избыточное питание мясопродуктами, содержащими большое количество нуклеиновых кислот, аминокислот и неорганических кислот, что делает такую пищу «кислой» и снижает рН мочи. Также кислотность мочи усиливается при ацидозах различного происхождения (Кислотно-основное состояние).
Кристаллы в почках могут иметь различную природу: 70-75% больных мочекаменной болезнью имеют камни щавелевой кислоты (оксалаты), 15% – мочевой кислоты, 10% – кальций-фосфатные, карбонатные, цистиновые камни. Самый большой почечный камень был извлечен 29.12.1952 из почки 80-летней женщины в Лондоне. Камень весил 6 кг 294 г.
Основы лечения
Так же, как при подагре, лечение сводится к беспуриновой диете и использованию аллопуринола. В дополнение рекомендуется растительная диета, приводящая к защелачиванию мочи, что увеличивает в моче долю более растворимой в воде енольной формы мочевой кислоты. Вместе с этим, уже имеющиеся кристаллы мочевой кислоты (а также кристаллы оксалатов) способны растворяться при подщелачивании мочи.
Лекарственное лечение непременно должно сопровождаться соблюдением беспуриновой диеты с большим количеством чистой воды, в противном случае неизбежно появление ксантиновых кристаллов в тканях и ксантиновых камней в почках.
Синдром Леша-Нихана
Болезнь Леша-Нихана (частота 1:300000) – это полное врожденное отсутствие активности гипоксантин-гуанин-фосфорибозил-трансферазы, фермента, отвечающего за реутилизацию пуриновых оснований. Признак рецессивный и сцеплен с Х-хромосомой. Впервые его описали в 1964 г в США студент-медик Майкл Леш и педиатр Уильям Нихан.
Дети рождаются клинически нормальными, только к 4-6 месяцу обнаруживаются отклонения в развитии, а именно – отставание физического развития (с трудом держит голову), повышенная возбудимость, рвота, периодическое повышение температуры. Выделение мочевой кислоты можно обнаружить еще раньше по оранжевой окраске пеленок. К концу первого года жизни симптомы нарастают, развивается нарушение координации движений, хореоатетоз, корковый паралич, спазм мышц ног. Наиболее характерный признак заболевания проявляется на 2-3-м году жизни – аутоагрессия или самокалечение – неодолимое стремление детей кусать себе губы, язык, суставы пальцев на руках и ногах. Агрессия больных распространяется также на неживые предметы и окружающих людей. Нарушения интеллекта выражены, его снижение может быть до IQ≈60.
Лечение основано на беспуриновой диете с большим количеством чистой воды и с использованием аллопуринола. Производится контроль деятельности пациента с помощью физических ограничений и психологической терапии.
Источник
Подагрическая нефропатия — это поражение почек, возникающее у больных подагрой. Может проявляться в разных вариантах, зачастую длительное время протекает бессимптомно. В последующем возможны почечные колики, дизурия, никтурия, олигурия, гематурия, боли в пояснице, артериальная гипертензия, спонтанное отхождение камней. Диагностируется с помощью определения уровня мочевой кислоты в моче и крови, УЗИ почек, исследования синовиальной жидкости, биоптатов суставных тканей и тофусов. Для лечения используют урикодепрессивные, урикозурические, урикоразрушающие препараты. По показаниям проводится массивная инфузионная терапия, заместительная терапия, хирургическое удаление камней.
Общие сведения
Подагрическая (мочекислая, уратная) нефропатия развивается у 30-70% пациентов с подагрой. Относится к категории собирательных понятий, объединяет все виды почечной патологии подагрического происхождения. Наиболее распространенной формой заболевания считается хронический интерстициальный нефрит, который у 17% больных на начальных этапах характеризуется эпизодами острой мочекислой обструкции почек и в 52% случаев сочетается с нефролитиазом.
В 30-40% урологическая патология является единственным проявлением нарушений метаболизма пуринов и служит «почечной» маской подагры. Как и основное заболевание, подагрическая нефропатия чаще выявляется у пациентов мужского пола. Актуальность своевременной диагностики нефрологического заболевания у больных, страдающих подагрой, связана с высоким риском развития ХПН.
Подагрическая нефропатия
Причины
Поражение почек при подагре провоцируется типичными для этого заболевания метаболическими нарушениями. Ключевым повреждающим фактором становится мочевая кислота, которая усиленно производится организмом больного из-за генетически обусловленной недостаточности фермента гипоксантин-гуанинфосфорибозилтрансферазы. Непосредственными причинами нефропатии являются:
- Гиперурикемия и урикозурия. Соли мочевой кислоты оказывают прямое токсическое воздействие на почечную паренхиму и вызывают обструкцию почечных канальцев, откладываясь в их просвете. Гиперурикемия также потенцирует усиление секреции ренина, фактора пролиферации сосудистых гладкомышечных волокон, тромбоксана.
- Кислая реакция мочи. При значительной урикозурии pH мочи может снижаться до 4,5-5,8, что облегчает преципитацию уратов в почках. Кислая моча усиливает дистрофию почечного эпителия, формирующуюся на фоне его постоянной травматизации камнями, становится питательной средой для размножения микроорганизмов.
Риск нефропатии при подагрическом процессе повышается у пациентов, которые злоупотребляют алкоголем, допускают погрешности в диете, употребляя в больших количествах мясо, бобовые и другие продукты, содержащие пурины. Уратное поражение почек чаще наблюдается у больных с абдоминальным ожирением, инсулинорезистентностью, сахарным диабетом. Провоцирующими факторами также могут стать длительное голодание, интенсивные тренировки и тяжелый физический труд, сопровождающиеся массивной анаэробной деструкцией белковых волокон. Уровень мочевой кислоты повышается при приеме салицилатов, диуретиков, ряда других лекарственных средств.
Патогенез
Механизм развития подагрической нефропатии основан на дисбалансе между высокой концентрацией мочевой кислоты и способностью к ее безопасной элиминации из организма. На фоне усиленного выделения мочевой кислоты клубочками и снижения pH мочи ураты начинают кристаллизоваться в почечных канальцах. В результате нарушается внутрипочечный пассаж мочи, усиливаются застойные явления, что опосредованно влияет на фильтрующую способность почек. Формирование и рост уратных конкрементов провоцируют дистрофические процессы в почечном эпителии.
Проникновение уратов в тубулоинтерстиций сопровождается воспалительной реакцией, усилением фиброгенеза, склерозированием паренхимы за счет образования соединительной ткани с последующим развитием почечной недостаточности. У части пациентов определенную роль в патогенезе нефропатии подагрического типа играют образование аутоиммунных комплексов, повреждающих мембраны клубочков, а также активация ренин-ангиотензиновой системы с возникновением артериальной гипертензии и нефроангиосклероза.
Классификация
Ключевыми критериями современной систематизации форм поражения почечных тканей при подагре являются тип морфологических изменений, острота течения и клиническая форма патологического процесса, этапность развития заболевания. У половины больных мочекислая нефропатия протекает по латентному типу с преимущественным поражением стромы, поздним появлением и медленным нарастанием симптоматики, у 30% — по острому или хроническому уролитиазному с повреждением канальцев, у 20% — по протеинурическому с преимущественным аутоиммунным поражением клубочкового аппарата.
Подагрическая нефропатия бывает острой и хронической. При остром уролитиазном процессе в канальцах, собирательных трубочках и почечных лоханках в большом количестве осаждаются кристаллы, что приводит к возникновению острой обструкции почек, болевому синдрому, в тяжелых случаях — острой почечной недостаточности. При подобном течении речь обычно идет об острой обструктивной мочекислой нефропатии.
Клинические варианты хронической подагрической почки соответствуют трем типам морфологических изменений почечной ткани. Соответственно специалисты в сфере урологии и нефрологии различают хронический тубулоинтерстициальный нефрит, уратный вариант мочекаменной болезни, подагрический гломерулонефрит. Более редкими формами нефрологической патологии у больных, которые страдают подагрой, являются тофусоподобные включения уратов в мозговое вещество почки и амилоидоз.
С лечебной и прогностической целью уточняют стадию хронического процесса. Постепенное нарушение функциональной состоятельности фильтрующего аппарата снижает компенсаторные возможностей почек по поддержанию нормальной концентрации мочевой кислоты, ухудшая прогноз заболевания. С учетом состояния клубочковой фильтрации выделяют три стадии развития хронической уратной нефропатии:
- I — подагрическая гиперурикозурия. Фильтрующая функция сохранена. В моче содержание мочевой кислоты обычно увеличенное, в крови — нормальное или слегка повышенное. Возможна микроальбуминурия. При правильно выбранной терапевтической тактике удается добиться стойкой коррекции состояния пациента.
- II — подагрическая гиперурикемия. Почки не справляются с повышенной уратной нагрузкой, нарушается осморегулирующая функция. Экскреция мочевой кислоты нормальная или незначительно повышена, ее содержание в крови существенно увеличено. Снижается плотность мочи. Прогноз становится более серьезным.
- III — подагрическая азотемия. Терминальная стадия заболевания, характеризующаяся наличием хронической почечной недостаточности. Лабораторное обследование выявляет высокую гиперурикемию, снижение суточной экскреции мочевой кислоты, повышение уровня креатинина в плазме крови.
Симптомы подагрической нефропатии
У 50% пациентов патология продолжительное время протекает латентно. Клиника зависит от формы и варианта течения мочекислой нефропатии. Для острой уратной обструкции характерно внезапное начало с возникновением интенсивной боли и тяжести в поясничной области, дизурическими явлениями, макрогематурией, резким уменьшением количества мочи. Почечная симптоматика нередко сочетается с подагрической суставной атакой. При уратном нефролитиазе с постепенным отложением солей и формированием камней периодически наблюдаются двухсторонние почечные колики с острой болью в области поясницы, иррадиирующей в бедро и пах, тошнотой и рвотой, напряжением мышц передней брюшной стенки, лихорадкой. Возможно спонтанное отхождение конкрементов.
При хроническом интерстициальном нефрите или гломерулонефрите основными проявлениями становятся стойкое повышение артериального давления, выявляемое у 70% пациентов, увеличение количества суточной мочи, усиление диуреза в ночное время. Изредка в моче появляется кровь. Симптоматика усугубляется при снижении фильтрующей функции подагрической почки: больных беспокоят постоянные ноющие боли, отмечаются расстройства мочеиспускания, гематурия, снижение объема мочи, выделенной за сутки. Важным признаком является красновато-бурый цвет мочи за счет окрашивания кристаллами мочекислого аммония.
Осложнения
При обструкции камнем мочеточника и затруднении пассажа мочи зачастую развивается гидронефроз с расширением чашечно-лоханочной системы и атрофией паренхимы почки. Повышенная продукция ренина при нефропатии приводит к стойкой артериальной гипертензии, которая с трудом поддается лечению. Вследствие застоя мочи происходит обсеменение мочевыделительного тракта микроорганизмами, у 75% больных возникает вторичный пиелонефрит. Серьезными осложнениями являются острая почечная недостаточность, требующая экстренной терапии, и нарастающая хроническая почечная недостаточность.
Диагностика
Диагностический поиск при подозрении на подагрическую нефропатию направлен на выявление характерных метаболических нарушений, возможных признаков уролитиаза, оценку функциональной состоятельности почек, исключение гиперурикемических расстройств неподагрического происхождения. Наиболее информативными для постановки диагноза являются:
- Определение содержания мочевой кислоты. Соответственно стадии уратной нефропатии может определяться гиперурикозурия (> 1100 мг/сут), гиперурикемия (> 500 мкмоль/л). Исследование дополняют общим анализом мочи, в котором выявляется стойко-кислая pH. У 67% пациентов снижена относительная плотность мочи (<1018), у 71% наблюдается протеинурия (<1г/л), у 37% — микрогематурия. Возможна лейкоцитурия, кристаллурия.
- УЗИ. При ультразвуковом исследовании почек эхо-признаки повреждения почечных структур обнаруживаются у 78,5% больных. Наиболее часто визуализируются конкременты, причем в трети случаев подагрический нефролитиаз является двухсторонним. Иногда просматривается от 1 до 3 почечных кист диаметром 0,5-4,0 см. Диагностическая ценность сонографии особенно высока с учетом рентген-негативности уратных камней.
- Исследование синовиальной жидкости. Метод поляризационной микроскопии применим при наличии суставной симптоматики. С его помощью в биологическом материале удается выявить внутриклеточные кристаллы мочевой кислоты, а также исключить другие причины болевого синдрома. Иногда более информативными оказываются биопсия тофусов (при их наличии), синовиальной оболочки и хряща пораженного сустава.
Для оценки фильтрующей функции проводится проба Реберга, назначается комплексный биохимический анализ крови (определение содержания креатинина, мочевины, калия, кальция, натрия, неорганического фосфора в сыворотке крови), лабораторный нефрологический комплекс (почечные пробы в моче). Из инструментальных методов могут применяться нефросцинтиграфия, экскреторная урография.
Подагрический вариант нефропатии дифференцируют с поражением почек при вторичных гиперурикемиях, вызванных бериллиозом, хронической свинцовой интоксикацией, саркоидозом, цистинозом, поликистозной болезнью, распространенным псориазом, миелопролиферативной болезнью, гипотиреозом, алкогольной зависимостью. Исключаются лекарственно-индуцированные гиперурикемические состояния, связанные с приемом тиазидных и петлевых диуретиков, нестероидных противовоспалительных средств, антибиотиков, цитостатиков, некоторых других препаратов. Кроме уролога или врача-нефролога по показаниям пациента консультирует ревматолог, дерматолог, эндокринолог, инфекционист, онколог, онкогематолог, токсиколог.
Лечение подагрической нефропатии
Основными терапевтическими задачами являются уменьшение синтеза мочевой кислоты, нефропротекция, улучшение почечной микроциркуляции, замедление прогрессирующего нефросклероза. Медикаментозное лечение обязательно дополняют коррекцией двигательного активности, питьевого режима и рациона. Пациентам с подагрическим поражением почек показаны минимально калорийные диеты с низким содержанием белка, частое щелочное питье, умеренные физические нагрузки для снижения веса. При выборе препаратов для терапии мочекислой нефропатии учитывают форму и стадию заболевания.
Схема ведения больных с острой уратной нефропатией аналогична терапии ОПН. При проходимости мочеточников и отсутствии анурии показана непрерывная инфузионная терапия под контролем диуреза с введением моносахаридов, многоатомных спиртов, физиологического или полиионных кристаллоидных растворов, петлевых диуретиков. Одновременно назначается обезболивание алкалоидами трополонового ряда, применяются ингибиторы ксантиноксидазы. Неэффективность интенсивного консервативного лечения, проводимого в течение 60 часов, является показанием для перевода пациента на гемодиализ.
Больным с хронической подагрической почкой проводится терапия, позволяющая откорректировать концентрацию мочевой кислоты, предупредить развитие возможных осложнений. При подборе препарата обязательно учитывают стадию патологического процесса и сохранность фильтрующей функции. Наиболее часто для лечения мочекислой нефропатии используют:
- Урикодепрессивные препараты. Ингибиторы ксантиноксидазы, глютаминфософорибозилтрансферазы и в меньшей степени карбоновые конъюгаторы фосфорибозилпирофосфата влияют на обмен ксантинов, нарушают синтез мочевой кислоты. За счет эффективного снижения гиперурикемии уменьшают выраженность урикозурии, а значит – и риск камнеобразования. Обладают умеренным нефропротективным эффектом: снижают выраженность протеинурии, синтез ренина, продукцию свободных радикалов, замедляют гломерулосклероз и нефроангиосклероз. Не рекомендованы при наличии ХПН.
- Урикозурические средства. За счет угнетения реабсорбции уратов усиливают экскрецию мочевой кислоты, однако увеличивают нагрузку на почки. Показаны при сочетании гиперурикемии с нормальным содержанием мочекислых солей в моче, отсутствии камней и сохраненной фильтрующей функции. С учетом индивидуальной чувствительности и возможных противопоказаний больным с подагрической почкой назначают производные и аналоги сульфинпиразона, цинхофена, пробенецида, 5-хлоробензоксазола, кебузона. Часть этих препаратов обладает умеренным диуретическим эффектом.
При наличии уролитиаза для растворения уратных конкрементов применяют урикоразрушающие средства на основе солей лития, пиперазина, фермента уратоксидазы, цитратных смесей. Эффективно сочетание основных противоподагрических препаратов с фитоуроантисептиками, предотвращающими пиелонефрит, физиотерапевтическими методиками (фототерапией, магнитотерапией, электроимпульсной терапией), санаторно-курортным оздоровлением.
При нарастании ХПН проводится заместительная почечная терапия (гемодиализ, перитонеальный диализ, гемофильтрация, гемодиафильтрация). Пациентам с крупными конкрементами, нарушающими пассаж мочи и раздражающими паренхиму, показана нефролитотомия, пиелолитотомия, перкутанная или дистанционная нефролитотрипсия.
Прогноз и профилактика
Болезнь характеризуется рецидивирующим течением с периодами обострения и ремиссии. Прогноз серьезный, в большинстве случаев через 10-12 лет от начала заболевания развивается ХПН. Для профилактики подагрической нефропатии пациентам с наследственной предрасположенностью рекомендуется соблюдать диету с ограничением мясных продуктов, животных жиров, копченостей, бобовых, из которых могут образоваться ураты, проходить скрининговые обследования с целью выявления патологии на ранней (бессимптомной) стадии.
Больным с диагностированной подагрой необходимо адекватное лечение основного заболевания, строгое соблюдение рекомендаций ревматолога по коррекции образа жизни и веса, отказ от алкоголя, осторожный подход при приеме препаратов, провоцирующих гиперурикемию, исключение чрезмерных физических нагрузок.
Источник


