Язвенный колит и язвенная болезнь желудка
Энциклопедия / Заболевания / Желудочно-кишечный тракт / Неспецифический язвенный колит (НЯК)
Неспецифический язвенный колит (НЯК) – хроническое воспалительное заболевание толстого кишечника, характеризующееся прогрессирующим течением и образованием язвенных дефектов.
По протяженности патологического процесса выделяют:
- проктит – легкая форма заболевания, воспалительные изменения затрагивают только прямую кишку;
- проктосигмоидит – средняя степень тяжести, заболевание прямой и сигмовидной кишки;
- тотальный колит – тяжелая форма, характеризующаяся поражением всей толстой кишки.
По течению выделяют острое, хроническое непрерывное и хроническое рецидивирующее течение болезни.
Причины заболевания до сих пор не установлены, хотя исследования постоянно ведутся. В разное время предположительными факторами развития НЯК считались различные бактерии, вирусы, токсины, психогенные факторы, влияние окружающей среды (жители сельской местности болеют реже, чем горожане), аутоиммунные механизмы, генетическая предрасположенность.
Следует отметить, что курение снижает риск развития данного заболевания.
Симптомы неспецифического язвенного колита зависят от протяженности патологического процесса и выраженности воспалительных изменений.
Местные симптомы:
- появление примеси крови на оформленном кале,
- ложные позывы на дефекацию (особенно по ночам),
- диарея при распространенном процессе (частота стула в тяжелых случаях может достигать 10 – 20 раз в сутки),
- наличие слизи и гноя в стуле,
- запоры (в случае поражения только прямой кишки),
- боли в животе.
При распространенном НЯК характерно присоединение общих симптомов:
- интоксикация,
- общая слабость,
- похудение,
- отсутствие аппетита,
- тошнота,
- выраженная эмоциональная неустойчивость.
Возможно появление системных проявлений:
- узловая эритема,
- полиартрит,
- поражения глаз, печени,
- стоматит, глоссит, гингивит.
В случае тяжелого течения болезни возможно развитие осложнений:
- кишечные кровотечение,
- разрыв стенки кишки,
- образование свищей и абсцессов,
- формирование рубцовых сужений кишечника с развитием непроходимости.
При подозрении на наличие у пациента неспецифического язвенного колита необходимо провести ряд обследований:
- общеклинические: общий анализ крови и мочи, ЭКГ, флюорография, измерение артериального давления, пульса, определение группы крови и резус-фактора
- развернутый биохимический анализ крови (глюкоза, билирубин+фракции, общий белок+фракции, мочевина, креатинин, АЛТ, АСТ, ГГТФ, ЩФ, железо, СРБ, калий, натрий)
- рентгенологические исследования: обзорный снимок органов брюшной полости и малого таза, рентгенография толстой кишки с контрастированием
- эндоскопические методы: колоноскопия с биопсией, ректороманоскопия, гастроскопия
- анализ кала на скрытую кровь и его клинический анализ (копрограмма)
Дифференциальная диагностика проводится с такими заболеваниями, как
- болезнь Крона,
- хронический (неязвенный) колит,
- синдром раздраженного кишечника,
- заболевания печени, поджелудочной железы, желчевыводящих путей.
*свериться с Федеральными рекомендациями по лечению и диагностике >>>
Одни и те же симптомы могут быть признаками разных заболеваний, а болезнь может протекать не по учебнику. Не пытайтесь лечиться сами — посоветуйтесь с врачом.
Лечением НЯК занимается гастроэнтеролог и хирург при осложнениях.
Питание
Важную роль в терапии играет диета с механический и химическим щажением, с увеличением потребления белка, снижением жира до 60-80 г в сутки, с максимальным ограничением клетчатки.
Медикаментозная терапия
Основными группами препаратов для лечения неспецифического язвенного колита являются:
сульфаниламиды:
препараты 5-аминосалициловой кислоты (5-АСК):
- салофальк для перорального применения, а также в свечах и растворе для клизм;
- пентаса
глюкокортикостероиды:
будесонид для местного применения,
- преднизолон в виде свечей,
- при неэффективности и большой протяженности патологического процесса преднизолон используется системно (перорально или парентерально)
антибиотики и противопротозойные средства:
в тяжелых случаях при неэффективности ГКС и 5-АСК к лечению подключают цитостатики:
- азатиоприн,
- циклоспорин
новые препараты – селективные иммуносупрессоры:
вспомогательные средства:
- антациды,
- ферменты
Хирургическое лечение
Удаление части толстого кишечника проводят при осложнениях и неэффективности консервативной терапии.
Современные методы лечения оказываются эффективными у 85% больных с легким или среднетяжелым течением неспецифического язвенного колита.
У большинства пациентов удается достичь полной ремиссии.
Умеренно выраженные клинические проявления сохраняются у 10% больных.
Раздел по диагностике и лечению неспецифического язвенного колита написана в соответствии с Федеральными рекомендациями.
Источник: diagnos.ru
Источник
ßçâåííûé êîëèò è ÿçâà æåëóäêà
ßçâåííûå ïîðàæåíèÿ â ïèùåâàðèòåëüíîì òðàêòå ïîäðàçäåëÿþòñÿ, â çàâèñèìîñòè îò ëîêàëèçàöèè, íà äâà çàáîëåâàíèÿ ÿçâåííûé êîëèò (â íèæíèõ îòäåëàõ) è ïåïòè÷åñêóþ ÿçâó (â âåðõíèõ).
ßçâåííûé êîëèò õðîíè÷åñêîå âîñïàëèòåëüíîå çàáîëåâàíèå, êîòîðîå ïîðàæàåò ñëèçèñòóþ îáîëî÷êó è ïîäñëèçèñòóþ òîëñòîé è ïðÿìîé êèøêè. Áîëåå âñåãî åé ïîäâåðæåíû ëþäè â âîçðàñòå 1530 ëåò. Òî÷íûå ïðè÷èíû âñå åùå íå ÿñíû, îäíàêî íàáëþäàåòñÿ âëèÿíèå ãåíåòè÷åñêèõ è èììóíîëîãè÷åñêèõ ôàêòîðîâ, èíôåêöèîííûõ àãåíòîâ, êóðåíèÿ, ëåêàðñòâåííûõ ñðåäñòâ. Åñòü èññëåäîâàíèÿ, ïîêàçûâàþùèå óâåëè÷åíèå ðèñêà çàáîëåòü ÿçâåííûì êîëèòîì, åñëè â îðãàíèçì â èçáûòêå ïîïàäàþò àëþìèíèé (ñ ïðîäóêòàìè, ïðèãîòîâëåííûìè â àëþìèíèåâîé ïîñóäå, íàïðèìåð çàâîäñêèì õëåáîì; ñ ïèòüåâîé âîäîé), ìàëüòîäåêñòðèí è êðàõìàë (âûïå÷êà, êðóïû), ñàõàðîçà.
Ê ñèìïòîìàì ÿçâåííîãî êîëèòà îòíîñÿòñÿ êðîâàâûé ïîíîñ, âêðàïëåíèÿ ãíîÿ, ñëèçè â êàëå è ñïàñòè÷åñêèå áîëè â æèâîòå âî âðåìÿ äåôåêàöèè. Êàê ïðàâèëî, ïðèñòóïû çàáîëåâàíèÿ ÷åðåäóþòñÿ ñ îòíîñèòåëüíûì çàòèøüåì.  èññëåäîâàòåëüñêîé ëèòåðàòóðå ìîæíî âñòðåòèòü ðåçóëüòàòû, ñâèäåòåëüñòâóþùèå î áëàãîòâîðíîì âëèÿíèè ïðîàíòîöèàíèäèíîâ èç âèíîãðàäíûõ ñåìå÷åê, êîòîðûå îáëàäàþò âûðàæåííûìè ïðîòèâîâîñïàëèòåëüíûìè ñâîéñòâàìè. Çåëåíûé ÷àé ïðè ÿçâåííîì êîëèòå îáëåã÷àåò ñèìïòîìû äèàðåè è ïîòåðè âåñà. Ðàíäîìèçèðîâàííîå, ïëàöåáî-êîíòðîëèðóåìîå èññëåäîâàíèå äâîéíûì ñëåïûì ìåòîäîì ëèñòüåâ àëîý âåðà ïîêàçàëî èõ ïîëåçíîñòü ïðè ýòîì çàáîëåâàíèè. Ïðîòèâîÿçâåííóþ àêòèâíîñòü èìååò àìèíîêèñëîòà ãëèöèí (åå ñîäåðæàò âñå áåëêîâûå ïðîäóêòû, íî áîëüøå âñåãî õðÿùè, æåëàòèí, à òàêæå ðûáà, ÿéöà), ìèêðîýëåìåíò ìîëèáäåí (ëèñòîâûå îâîùè, áîáîâûå, îãóðöû, ìîðêîâü, ÷åñíîê), ïîëèñàõàðèä èíóëèí (òîïèíàìáóð, öèêîðèé, áàíàíû, ëóê è ÷åñíîê).
Åùå îäíà áîëåçíü ïåïòè÷åñêàÿ ÿçâà æåëóäêà è äâåíàäöàòèïåðñòíîé êèøêè ÿâëÿåòñÿ îäíèì èç ñàìûõ ðàñïðîñòðàíåííûõ çàáîëåâàíèé â ìèðå. Ðàçâèòèå ýòîé áîëåçíè ñâÿçûâàþò ñ íàðóøåíèå áàëàíñà «çàùèòíûõ» è «àãðåññèâíûõ» ôàêòîðîâ, âëèÿþùèõ íà öåëîñòíîñòü ñëèçèñòîé îáîëî÷êè. Ê àãðåññèâíûì ôàêòîðàì, â ÷àñòíîñòè, îòíîñÿòñÿ ïîâûøåííàÿ êèñëîòíîñòü æåëóäî÷íîãî ñîêà (èçáûòîê ïðîäóêöèè ñîëÿíîé êèñëîòû), àêòèâíîñòü ôåðìåíòà ïåïñèíà, äåéñòâèå æåë÷íûõ êèñëîò, íåñòåðîèäíûõ ïðîòèâîâîñïàëèòåëüíûõ ïðåïàðàòîâ (àñïèðèí), èøåìèÿ è ãèïîêñèÿ ñëèçèñòîé, êóðåíèå, çëîóïîòðåáëåíèå àëêîãîëåì è ðàçìíîæåíèå âðåäîíîñíîé áàêòåðèè Helicobacter pylori. Çàùèòíûå ôàêòîðû âêëþ÷àþò ïðèñòåíî÷íîå îáðàçîâàíèå áèêàðáîíàòîâ, òîëùèíó ñëèçè, èíòåíñèâíîñòü êðîâîòîêà â ñëèçèñòîé, ïðîñòàãëàíäèíû è ôàêòîðû ðîñòà.
Ðèñê çàáîëåòü âîçðàñòàåò:
ïîñëå 65 ëåò;
ïðè ñèñòåìàòè÷åñêîì ïðèåìå íåñòåðîèäíûõ ïðîòèâîâîñïàëèòåëüíûõ ïðåïàðàòîâ;
ïðè óïîòðåáëåíèè ñòåðîèäíûõ ïðåïàðàòîâ;
ïðè ïðèåìå àíòèäåïðåññàíòîâ (èíãèáèòîðîâ îáðàòíîãî çàõâàòà ñåðîòîíèíà).
×àùå âñåãî ÿçâà æåëóäêà âîçíèêàåò ó ëþäåé, ñòðàäàþùèõ îñòåîàðòðèòîì è ðåâìàòîèäíûì àðòðèòîì. Ýòî ñâÿçàíî, ïî-âèäèìîìó, ñ òåì, ÷òî îíè âûíóæäåíû ïðèíèìàòü íåñòåðîèäíûå ïðîòèâîâîñïàëèòåëüíûå ïðåïàðàòû.
Íåáîëüøèå ÿçâû ìîãóò íå âûçûâàòü íèêàêèõ ñèìïòîìîâ, îäíàêî áîëüøèå ñïîñîáíû ïðèâîäèòü ê ñåðüåçíûì êðîâîòå÷åíèÿì. Ïåðå÷èñëèì íåêîòîðûå ñèìïòîìû ýòîé áîëåçíè:
îùóùåíèå ïåðåïîëíåííîñòè æåëóäêà, íåâîçìîæíîñòü ïèòü ìíîãî æèäêîñòè;
ãîëîä è îùóùåíèå ïóñòîòû â æåëóäêå ñïóñòÿ 13 ÷àñà ïîñëå åäû;
ëåãêàÿ òîøíîòà è ðâîòà.
áîëü èëè äèñêîìôîðò â âåðõíåé ÷àñòè æèâîòà;
áîëü â âåðõíåé ÷àñòè æèâîòà, êîòîðàÿ áóäèò âàñ â íî÷íîå âðåìÿ.
Äîïîëíèòåëüíûìè ñèìïòîìàìè ìîãóò áûòü: êðîâàâûé èëè òåìíûé ñòóë, áîëü â ãðóäè, óòîìëÿåìîñòü, ðâîòà, ïîòåðÿ âåñà.
Ìàñëî è ñëèçü èç ñåìÿí ëüíà îêàçûâàþò çàùèòíîå äåéñòâèå ïðè ÿçâå æåëóäêà. Àëêîãîëüíûé ýêñòðàêò ëèñòüåâ àëîý, êóðêóìû èëè ïëîäîâ ãâîçäè÷íîãî äåðåâà, âîäíûå ýêñòðàêòû àïòå÷íîé ðîìàøêè, ìåëèññû, òìèíà, ïåðå÷íîé ìÿòû, ëàêðèöû, ðàñòîðîïøè ïîêàçàëè îáíàäåæèâàþùèå ðåçóëüòàòû â èññëåäîâàíèÿõ çàæèâëåíèÿ èíäóöèðîâàííûõ ÿçâ íà êðûñàõ. Ïðè ýòîì ñíèæàëàñü êèñëîòíîñòü æåëóäî÷íîãî ñîêà, óâåëè÷èâàëîñü îáðàçîâàíèå ñëèçè, ïîâûøàëîñü âûñâîáîæäåíèå ïðîñòàãëàíäèíà E2 è ñíèæàëîñü îáðàçîâàíèå ãàñòðèíà è ëåéêîòðèåíîâ. Ýôôåêòû ýòèõ ðàñòåíèé ñâÿçûâàþò ñ íàëè÷èåì â íèõ ïðîòèâîâîñïàëèòåëüíûõ è àíòèîêèñëèòåëüíûõ ïîëèôåíîëîâ.
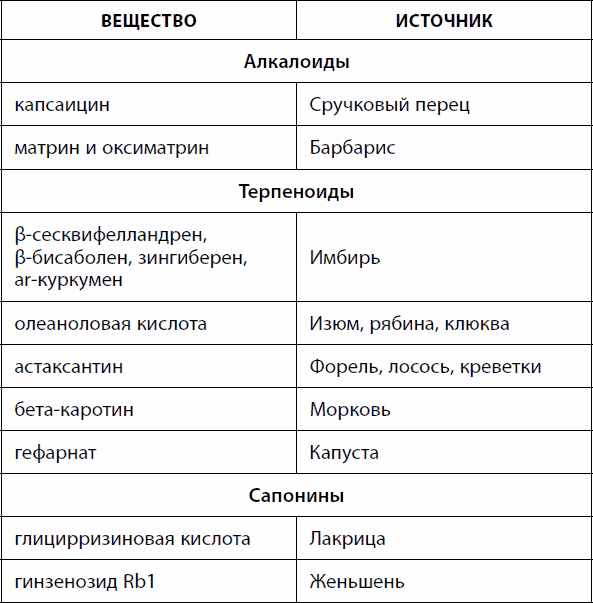
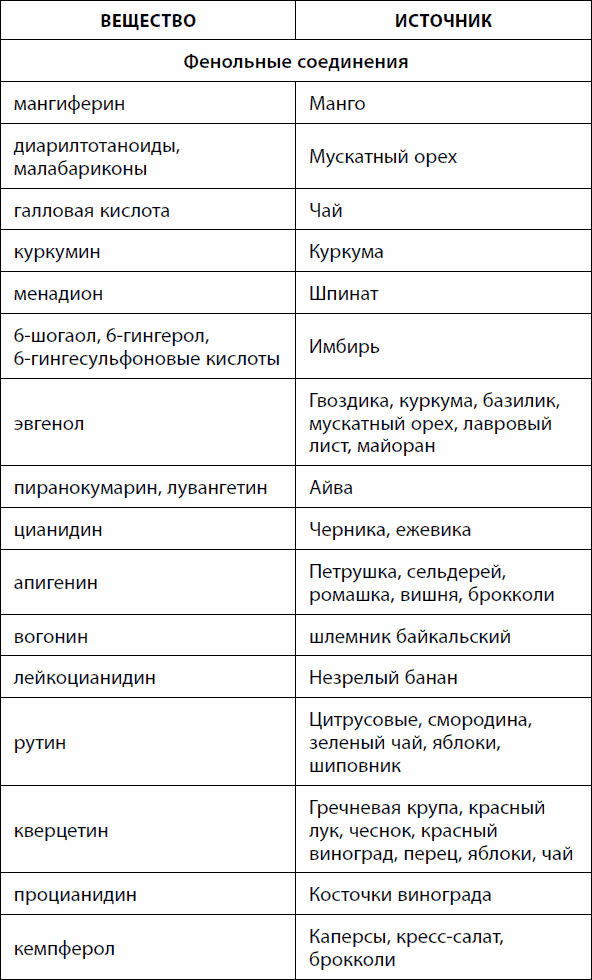
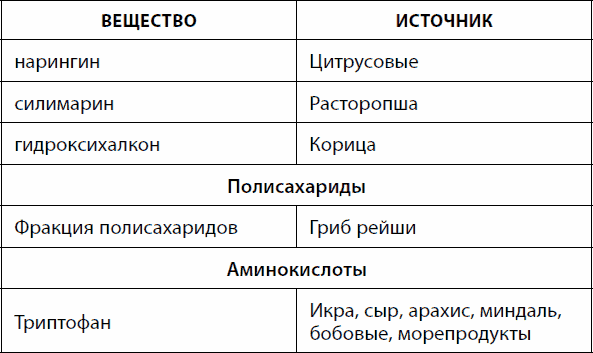
Ïðîòèâîÿçâåííûì äåéñòâèåì îáëàäàþò ìíîãèå ñîåäèíåíèÿ, âñòðå÷àþùèåñÿ â ïðîäóêòàõ íàøåãî ïèòàíèÿ (òàáë. 3).
Òàáëèöà 3. Ïðèðîäíûå âåùåñòâà ñ ýêñïåðèìåíòàëüíûìè ïðîòèâîÿçâåííûìè ýôôåêòàìè
Источник
Аутоиммунный гастрит.
Аутоиммунный гастрит относится к частым аутоиммунным заболеваниям и наиболее частым аутоиммунным заболеванием желудочно-кишечного тракта (ЖКТ). Этому заболеванию в 30% случаев сопутствуют другие аутоиммунные патологические состояния: аутоиммунные заболевания щитовидной железы, алопеция и витилиго. Аутоиммунный гастрит протекает субклинически и редко является поводом обращения пациентов к врачу. В его основе лежит аутоиммунная реакция, направленная против обкладочных (париетальных) клеток желудка, а также против внутреннего фактора (фактора Кастла). Обкладочных клеток больше в теле желудка, поэтому обычно аутоиммунный гастрит проявляется атрофией фундальных отделов, по сравнению с антральным гастритом при инфекции Helicobacter pylori. Для деффиринцаильной диагностики гастрита, ассоциированного с аутоиммунной реакцией и связанного с инфекцией Helicobacter pylori, используется тест Серологическое обследование гастритов типов А и В. Обкладочные клетки желудка вырабатывают соляную кислоту и внутренний фактор Кастла, необходимый для всасывания витамина В12 в кишечнике. Уничтожение обкладочных клеток ведет к гипоацидному гастриту, мальабсорбции, железодефицитной и пернициозной анемиям.
Антитела к обкладочным (париетальным) клеткам желудка.
Париетальные (обкладочные) клетки желудка вырабатывают соляную кислоту и внутренний фактор Кастла, необходимый для всасывания витамина В12 (кобаламина) в кишечнике. Основным антигеном антител к париетальным клеткам желудка (АПКЖ) является бета-субъединица Н+/К+ АТФ-азы, мембрано-ассоциированного ионного насоса, который участвует в закислении содержимого желудка. Аутоантитела являются комплемент-фиксирующими и непосредственно участвуют в разрушении популяции обкладочных клеток и развитии атрофического гастрита. Не отмечается взаимосвязи между обнаружением аутоантител к париетальным клеткам желудка и антральным гастритом, основной этиологической причиной которого является инфекция Helicobacter pylori. Титры аутоантител не коррелируют с тяжестью атрофии слизистой желудка, поэтому их мониторинг не целесообразен. Антитела к обкладочным клеткам желудка отмечаются у 90% больных с атрофическим гастритом и пернициозной анемией. Другие проявления дефицита витамина В12, обусловленные аутоиммунным гастритом, включают полиневрит, фуникулярный миелоз, атаксию, истощение мышц и снижение рефлексов. Нарушение закисления желудка приводит также к нарушению всасывания железа в тонком кишечнике, поэтому аутоиммунный гастрит, связанный с присутствием аутоантител к парительным клеткам желудка, может также приводить к развитию железодефицитной анемии с характерной клиникой этого состояния. Макроцитарная анемия обусловлена дефицитом эритропоэза в связи с нехваткой витамина В12. Анемия развивается через несколько лет после развития аутоиммунного гастрита, поскольку в норме в печени человека сохраняется значительный запас витамина. Анемия проявляется увеличением среднего размера эритроцита, повышением цветного показателя, характерными изменениями нейтрофилов, низким количеством ретикулоцитов, тромбоцитопенией и лейкопенией. Кроме того отмечается мегалобластная трансформация в костном мозге.
Антитела к внутреннему фактору (фактору Кастла).
Внутренний фактор (фактор Кастла) представляет собой гликопротеин массой 72 кДа, который секретируется в просвет желудка и связывает и транспортирует в стенку кишки витамина В12 (кобаламина). Аутоантитела к внутреннему фактору способны вызывать нарушение его функции как за счет блокады его связывания с витамином, так и препятствуя адсорбции комплекса в тонком кишечнике. Антитела к внутреннему фактору являются более специфичными по сравнению с антителами к парительным клеткам желудка при диагностике пернициозной анемии и дефицита витамина В12, однако встречаются только у 60% больных с аутоиммунным гастритом.
Комплексная оценка аутоантител при подозрении на аутоиммунный гастрит позволяет повысить точность лабораторной диагностики данного состояния (Диагностика гастрита типа А и пернициозной анемии).
Диагностика воспалительный заболеваний кишечника (болезнь Крона и язвенный колит).
Болезнь Крона (БК) и язвенный колит (ЯК) представляют собой хронические, рецидивирующие, идиопатические расстройства ЖКТ. При этом БК характеризуется иммунным, трансмуральным, сегментарным, гранулематозным воспалением ЖКТ различной протяженности от полости рта до анального отверстия, с развитием местных и системных осложнений, а ЯК — поражением только толстой кишки с обязательным вовлечением прямой, и воспаление при этом чаще всего ограничивается слизистой оболочкой кишечника и носит диффузный характер. Болезнь Крона и язвенный колит представляют собой наиболее частые формы ВЗК в европейской популяции и за последние несколько лет наблюдается стабильное повышение заболеваемости и распространенности данных заболеваний в развитых и развивающихся странах (5,6 на 100,000 в год в некоторых странах Европы). По данным Американского центра по эпидемическому контролю болезней примерно 1,4 млн. человек популяции США страдают от воспалительных заболеваний кишечника. В Германии распростраенность оценивается в пределах 1/500 до 1/800 взрослого населения. В Санкт-Петербурге по данным городского центра ВЗК на учете стоит 5,500 пациентов. Диагноз БК и ЯК, согласно международным и отечественным клиническим рекомендациям по диагностике и лечению ВЗК, устанавливается на основании всесторонней оценки клинической картины заболеваний, данных эндоскопических, радиологических, гистологических и лабораторных методов исследований. В 2011 году были опубликованы данные, рекомендующие рутинное использование панелей серологических маркеров для диагностики или мониторинга ВЗК в клинической практике. Но аутоантитела при ВЗК имеют ограниченную диагностическую ценность в первичной диагностике вследствие их низкой чувствительности.
Серологические маркеры диагностики болезни Крона. Антитела к пекарским дрожжам Sacchаromyces cerevisiae и антитела к экзокринной части поджелудочной железы и антигену GP2.
Антитела к пекарским дрожжам Sacchаromyces cerevisiae (ASCA) являются основным лабораторным маркером болезни Крона. Кроме антител к антигенам пекарских дрожжей, при болезни Крона появляются антитела к другим комменсальным организмам ЖКТ. Так, при этом заболевании появляются антитела антигенам кишечной палочки, псевдомонад, а также антигенам полисахаридной стенки многих микроорганизмов. Основными иммуногенными эпитопами антител к сахаромицетам являются также компоненты полисахаридов, в том числе маннотетроза и маннотриоза.
Антитела к сахаромицетам выявляются при болезни Крона с частотой, составляющей около 50% (30-70%). Антитела могут быть представлены IgG или IgA, обладая общей специфичностью для диагностики болезни Крона составляющей 93%. Частота выявления ASCA не зависит от географического района и демографии обследованных групп, что указывает на универсальность иммунологического механизма, лежащего в основе иммунной реакции против клеток сахаромицет. Характерно, что антитела к сахаромицетам часто отмечаются у родственников больных воспалительными заболеваниями кишечника (20-25%). У клинически здоровых лиц ASCA могут быть выявлены у 1-3% лиц общей популяции. При болезни Крона антитела к сахаромицетам могут появляться до клинического дебюта заболевания. При болезни Крона у пациентов с ASCA заболевание течет тяжелее, что связано с частыми эпизодами кишечной непроходимости, кроме того заболевание лучше отвечает на терапию блокаторами фактора некроза опухоли-альфа. В то же время, титры антител не коррелируют с клинической активностью процесса. Антитела к сахаромицетам могут использоваться для дифференциальной диагностики болезни Крона и неспецифического язвенного колита, поскольку встречаемость антител у больных с язвенным колитом не превышает 10%. Редко ASCA встречаются при первичном билиарном циррозе, первичном склерозирующем холангите, целиакии. Отсуствие антител к сахаромицетам (ASCA) не исключает вероятности болезни Крона.
Антитела к центроацинарным клеткам реагируют с цитоплазмой ацинарных клеток поджелудочной железы или с глобулярными структурами в протоках поджелудочной железы. Причина появления антител к ацинарным клеткам при БК остается неизвестной. Поражение поджелудочной железы иногда отмечается при ВЗК, однако не обнаружено взаимосвязи между панкреатитом и появлением антител к панкреоцитам. Вероятно, это связано с преимущественной экскрецией большинства антигенов в составе сока поджелудочной железы. Описано несколько антигенов ацинарных клеток, в частности гликопротеин GP2, который экскретируются поджелудочной железой в просвет кишечника. Антитела к экзокринной части поджелудочной железы отмечаются у 10-20% пациентов с болезнью Крона, несколько чаще у сравнительно молодых пациентов. Крайне редко антитела к центроацинарным клеткам поджелудочной железы могут отмечаться при других заболеваниях ЖКТ. Обнаружение антител к экзокринной части поджелудочной железы указывает на высокую вероятность БК и требует углубленного клинического и инструментального обследования. В сочетании с другими клиническими, инструментальными и лабораторными находками выявление антител позволяет поставить диагноз БК.
Изучение антигенных мишеней антител к центроацинарным клеткам привело к описанию белка GP2 (гликопротеина 2 типа) который является основным антигеном экскреторных гранул зимогенов. Обладая высокой структурной гомологией с белком Тамм-Хорсфала в моче, гликопротеин GP2 в просвете кишечника выполняет антибактериальную функцию, связываясь с фимбриями бактерий. Кроме того гликопротеин GP2 обладает антиапоптотическим и пролиферативным действием на энтероциты, таким образом, выступая в качестве протективного фактора. Антитела к GP2 классов IgGи IgA отмечаются у 30-35% пациентов с болезнью Крона, независимо от присутствия ASCA, поэтому совместное использование обоих маркеров позволяет выявить серологические признаки заболевания у 60-70% пациентов. Антитела к GP2 чаще отмечаются у более молодых больных.При БК антитела к GP2 антигену отмечаются при илиоколите, стриктурирующей формах заболевания с частым перианальным воспалением. Антитела к GP2 редко отмечаются у больных с неспецифическим язвенным колитом и менее чем у 3% здоровых лиц. Антитела к GP2 могут отмечаться при других заболеваниях ЖКТ, в том числе целиакии.
Серологические маркеры диагностики язвенного колита. Антитела к цитоплазме нейтрофилов (АНЦА) IgA и Антитела к бокаловидным клеткам кишечника (БКК).
Антинейтрофильные цитоплазматические антитела (АНЦА) были впервые описаны при гранулематозных васкулитах. При системных васкулитах в качестве основных антигенов антинейтрофильных антител выступает ряд ферментов содержащихся в азурофильных гранулах нейтрофилов. К известным антигенным мишеням АНЦА относятся протеиназа-3, миелопероксидаза, лактоферрин, эластаза, белок BPI и катепсин G. Антинейтрофильные антитела также используются в качестве диагностических маркеров при воспалительных заболеваниях кишечника, однако при этих заболеваниях большинство антигены аутоантител плохо изучено. Метод непрямой иммунофлюоресценции остается «золотым стандартом» выявления антинейтрофильных антител, поскольку позволяет определить как частые антигены (такие как протеиназа-3 или миелопероксидаза), так и редкие мишени аутоантител, которые охарактеризованы недостаточно хорошо. Для клинической диагностики воспалительных заболеваний кишечника целесообразно дополнять выявление антинейтрофильных антитела класса IgA выявлением антинейтрофильных цитоплазматических антител класса IgG.
Антитела к цитоплазме нейтрофилов часто отмечаются при аутоиммунной патологии желудочно-кишечного тракта. Они встречаются при язвенном колите (70%), болезни Крона (2-7%), аутоиммунном гепатите (50%), первичном склерозирующем холангите (40%), первичном биллиарном циррозе (5%), болезни Шенлейн-Геноха (70%) и васкулитах при ревматоидном артрите (5-10%). При неспецифическом язвенном колите выявление высоких титров антинейтрофильных антител отмечается у больных с тяжелым течением заболевания. Повышенный титр АНЦА IgA указывает на вероятный диагноз язвенного колита и ассоциированного с ним первичного склерозирующего холангита.
Бокаловидные клетки кишечника (БКК) вырабатывают слизь, которая защищает слизистую кишки от агрессивных факторов содержимого кишки. Такие клетки, имеющие форму чаши (бокала), можно обнаружить во всех отделах кишечника, однако их число максимально в прямой кишке, особенно в криптах толстого кишечника. Основным антигеном БКК являются муцины – семейство гликопротеинов, состоящие из белка и углеводной последовательности. Как центральный белок, так и углеводная цепь являются мишенью антител при неспецифическом язвенном колите (НЯК).
Наличие антител к БКК тесно связано с язвенным колитом. Антитела к БКК часто отмечаются у пациентов с ЯК 15-40%, редко встречаются при болезни Крона, других орган-специфических аутоиммунных заболеваниях и очень редко у здоровых лиц. Также антитела к БКК могут встречаться при аутоиммунной энтеропатии – редком состоянии, связанном со снижением числа бокаловидных клеток, виллезной атрофией и воспалением в тонком кишечнике. Аутоиммунная энтеропатия проявляется рецидивирующией диареей, нарушением всасывания, кроме того она часто бывает связана с другими аутоиммунными заболеваниями и полиэндокинопатиями. Другим важным серологическим тестом на аутоиммунную энтеропатию является Определение антител к энтероцитам методом непрямой иммунофлюоресценции для диагностики аутоиммунной энтеропатии.
Источник

